题目内容
15.下列事实中,能用同一化学原理解释的是( )| A. | 氯气和二氧化硫都能使品红溶液褪色 | |
| B. | 二氧化硫和乙烯都能使溴水溶液褪色 | |
| C. | 二氧化硫和乙烯都能使酸性高锰酸钾溶液褪色 | |
| D. | 大量Na2SO4和甲醛都能使蛋白质从溶液中析出 |
分析 A.二氧化硫与品红化合生成无色物质,而氯气与水反应生成的HClO,具有强氧化性;
B.二氧化硫和乙烯都能使溴水褪色,前者是氧化反应,后者是加成反应;
C.二氧化硫和乙烯都具有还原性,能够酸性的高锰酸钾氧化;
D.亚硫酸钠溶液使蛋白质产生盐析;甲醛使蛋白质变性.
解答 解:A.二氧化硫与品红化合生成无色物质,而氯气与水反应生成的HClO,具有强氧化性使品红褪色,则原理不同,故A错误;
B.二氧化硫和乙烯都能使溴水褪色,前者是氧化反应,后者是加成反应,二者原理不同,故B错误;
C.二氧化硫和乙烯都能使酸性高锰酸钾溶液褪色,都体现还原性,原理相同,故C正确;
D.亚硫酸钠溶液使蛋白质产生盐析;甲醛使蛋白质变性,二者原理不同,故D错误;
故选:C.
点评 本题考查了元素化合物知识,熟悉二氧化硫的性质是解题关键,注意蛋白质的盐析与变性的区别.

练习册系列答案
相关题目
6.A、B、C均为短周期元素,A、B同周期,A、C的最低价阴离子分别为A2-、C-,A2-离子半径大于C-,B2+与C-具有相同的电子层结构.下列叙述中一定不正确的是( )
| A. | 它们的原子序数A>B>C | B. | 它们的离子半径A2->C->B2+ | ||
| C. | 它们的原子半径C>B>A | D. | 它们的最外层电子数C>A>B |
3.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1L 1mol/L 盐酸中含有HCl分子数为 1NA | |
| B. | 常温常压下,22.4L氧气所含的原子数为2NA | |
| C. | 实验室分别用KClO3和H2 O2制取3.2g O2时,转移的电子数均为0.4NA | |
| D. | 常温常压下,16 g 由O2和O3组成的混合气体所含电子数为8NA |
20.已知一种c(H+)=1×10-3 mol/L的一元酸溶液和一种c(OH-)=1×10-3mol/L的一元碱溶液等体积混合后溶液呈碱性,生成的盐可能是( )
| A. | 强酸强碱盐 | B. | 强酸弱碱盐 | ||
| C. | 强碱弱酸盐 | D. | 上述三种盐均可能 |
7.改变外界条件可以影响化学反应速率,针对H2(g)+I2(g)?2HI(g),其中能使活化分子百分数增加的是
①增加反应物浓度 ②增大气体的压强 ③升高体系的温度 ④使用催化剂( )
①增加反应物浓度 ②增大气体的压强 ③升高体系的温度 ④使用催化剂( )
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
5.下列关于指定粒子的构成叙述中,正确的是( )
| A. | 37Cl与39K所含的中子数不同 | |
| B. | 12C和14C是不同的核素,但质子数相等 | |
| C. | H3O+与OH-的质子数和电子数均相同 | |
| D. | Mg2+与O2-的核外电子排布不相同 |
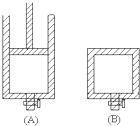 有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).
有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).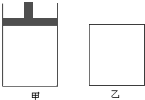 将4mol SO2与2mol O2的混合气分别置于容积相等的甲、乙两容器中,发生反应:2SO2(g)+O2(g)?2SO3(g);△H<0,在相同温度下使其均达到平衡状态.甲是恒压容器,乙是恒容容器.甲容器达到平衡状态时,测得混合气体的物质的量为4.2mol;乙容器经50s达到平衡状态.请回答:
将4mol SO2与2mol O2的混合气分别置于容积相等的甲、乙两容器中,发生反应:2SO2(g)+O2(g)?2SO3(g);△H<0,在相同温度下使其均达到平衡状态.甲是恒压容器,乙是恒容容器.甲容器达到平衡状态时,测得混合气体的物质的量为4.2mol;乙容器经50s达到平衡状态.请回答: ;
;