题目内容
20.下列热化学方程式:Zn(s)+$\frac{1}{2}$O2(g)=ZnO(s)△H1=-351.1kJ/mol;
Hg(l)+$\frac{1}{2}$O2(g)=HgO(s)△H2=-90.7kJ/mol.
由此可知:Zn(s)+HgO(s)=ZnO(s)+Hg(l)△H3=-260.4kJ•mol-1.
分析 由盖斯定律,反应热与反应的途径无关,只与起始状态、最终状态有关,由已知热化学方程式乘以合适的系数进行适当的加减,反应热也乘以相应的系数进行相应的加减,据此计算.
解答 解:由①Zn(s)+$\frac{1}{2}$O2(g)=ZnO(s)△H=-351.1kJ•mol-1,
②Hg(1)+$\frac{1}{2}$O2(g)=HgO(s)△H=-90.7kJ•mol-1,
则根据盖斯定律可知,①-②得Zn(s)+HgO(s)═ZnO(s)+Hg(1),
所以△H=(-351.1kJ•mol-1)-(-90.7kJ•mol-1)=-260.4 kJ•mol-1,
故答案为:-260.4kJ•mol-1.
点评 本题考查学生利用盖斯定律计算反应热,题目难度不大,关键在于设计反应过程,构造出目标反应式.

练习册系列答案
相关题目
10.下列反应属于吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 酸碱中和的反应 | |
| C. | 甲烷在氧气中的燃烧反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
11.下列关于物质的量浓度表述中正确的是( )
| A. | 0.3 mol•L-1 Na2SO4溶液中含有Na+和SO42-总物质的量为0.9 mol | |
| B. | 当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol•L-1,只有当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol•L-1 | |
| C. | 在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量浓度相等,则K+和Cl-的物质的量浓度一定相同 | |
| D. | 10℃时0.35 mol•L-1的KCl饱和溶液100 mL,蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol•L-1 |
12.在下列各溶液中,离子一定能大量共存的是( )
| A. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- | |
| B. | 碱性溶液中:K+、Mg2+、S2-、ClO- | |
| C. | 加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- | |
| D. | 在AlCl3溶液中:K+、Na+、SiO32-、SO42- |
9.下列说法正确的是( )
| A. | 煤的主要组成为苯以及苯的同系物 | |
| B. | “可燃冰”为水可能变成油提供了有力的证据 | |
| C. | 油脂、淀粉、纤维素、蛋白质都是高分子化合物 | |
| D. | 石油的裂解是使石油分馏产物中的长链烃断裂成乙烯、丙烯等气态短链烃 |
10.下列离子组能大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、Mg2+、OH-、NO3- | ||
| C. | Na+、H+、CO32-、Fe2+ | D. | Mg2+、Cu2+、Cl-、SO42- |
 三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.
三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.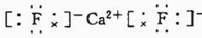 .
.