题目内容
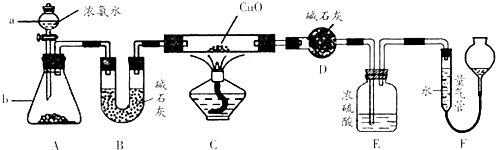
某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
(1)仪器a的名称为________;仪器b中可选择的试剂为________;

(2)实验室中利用下列各组物质,进行喷泉实验,不能成功的是( )
A.Cl2与饱和食盐水 B.CO2 与40%的NaOH溶液
C.NH3与饱和食盐水 D.HCl与水
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有还原性,写出相应的化学方程式______________________________ .
(4)E装置中浓硫酸的作用_______________________
(5)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为________(用含m、n字母的代数式表示)
(1)分液漏斗 氧化钙或氢氧化钙或碱石灰
(2)A
(3)3CuO + 2NH3 3Cu
+ N2↑ + 3H2O
3Cu
+ N2↑ + 3H2O
(4)吸收未反应的氨气,阻止F中水蒸气进入D
(5)9n/11.2m
【解析】
试题分析:(1)实验室中常用浓氨水加热或将浓氨水滴加到固体氧化钙或氢氧化钙上,利用氧化钙或氢氧化钙的吸水性及溶解放热来促使氨气溢出。(2)进行喷泉实验成功的关键是气体在液体中溶解度大。产生于外界足够大的压强差。Cl2在饱和食盐水溶解的少,不能形成压强差。进行喷泉实验,不能成功。其它选项都可以。(3)NH3和CuO加热时发生氧化还原反应的方程式是:3CuO + 2NH3 3Cu
+ N2↑ + 3H2O(4)E装置中浓硫酸的作用是吸收未反应的氨气,阻止F中水蒸气进入D . (5)干燥管D增重mg,即吸收水蒸气的质量是mg,装置F测得气体的体积为nL,就是N2在标准状况体积是nL。n(H2O):n(N2)=(mg÷18g/mol):(nL÷22.4L/mol)=11.2m:9n. 则氨分子中氮、氢的原子个数比为(9n×2): (11.2m×2)= 9n/11.2m
3Cu
+ N2↑ + 3H2O(4)E装置中浓硫酸的作用是吸收未反应的氨气,阻止F中水蒸气进入D . (5)干燥管D增重mg,即吸收水蒸气的质量是mg,装置F测得气体的体积为nL,就是N2在标准状况体积是nL。n(H2O):n(N2)=(mg÷18g/mol):(nL÷22.4L/mol)=11.2m:9n. 则氨分子中氮、氢的原子个数比为(9n×2): (11.2m×2)= 9n/11.2m
考点:考查仪器的识别、应用和氨气的实验室制法及性质等知识。

 某课外活动小组欲利用下列装置(部分固定装置略)完成下列实验;
某课外活动小组欲利用下列装置(部分固定装置略)完成下列实验;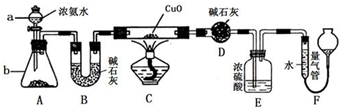 某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如图实验(夹持装置未画出)进行实验.请回答下列问题:
某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如图实验(夹持装置未画出)进行实验.请回答下列问题: