(10分)利用光能和光催化剂,可将CO
2和H
2O(g)转化为CH
4和O
2。紫外光照射时,在不同催化剂(I ,II,III)作用下,CH
4的产量随光照时间的变化如下图所示。

(1) 在O?30小时内,CH
4的平均生成速率

和

由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH
4最多。
(2) 将所得CH
4与H
2O(g)通入聚焦太阳能反应器,发生反应
CH
4(g)+H
2O(g)

CO(g) +3H
2(g) △H=+206kJ·mol
-1。将等物质的量的CH
4和H
2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH
4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。
(3) 该反应产生的CO和H
2可用来合成可再生能源甲醇,已知CO(g)、CH
3OH⑴的燃烧热

分别为
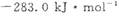
和

,则CH
3OH(l)不完全燃烧生成CO(g)和H
2O(l)的热化学方程式为_________。
(4)工业上常利用反应CO(g)+2H
2(g)

CH
3OH (g), △H<0合成甲醇,在230°C?270°C最为有利。为研究合成气最合适的起始组成比n(H
2):n(C0),分别在230°C、250
0C和270
0C进行实验,结果如图。

①270
0C的实验结果所对应的曲线是_________ (填字母);
②230
0C时,工业生产适宜釆用的合成气组成n(H
2):n(CO)的比值范围是_________ (填字母)。
A. 1 ?1.5 B. 2. 5?3 C. 3. 5?4. 5
(5) 某同学以石墨为电极,以KOH溶液为电解质设计甲醇燃料电池,其负极的电极反应式为_________。





 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案