题目内容
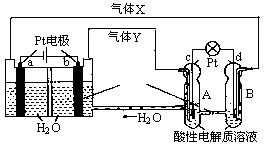
在生产和生活中金属腐蚀难以避免。对图a和图b的分析合理的是
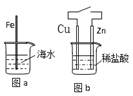

| A.图a,负极上发生的反应是:O2+4e+2H2O → 4OH- |
| B.图b,接通开关后溶液中的H+向正极移动 |
| C.图a,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D.图b,接通开关后Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
B
试题分析:A、负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-=Fe2+,故A错误;B、原电池放电时,阳离子流向正极,所以溶液中的H+向正极移动,故B正确;C、插入海水中的铁棒,在液面与空气的交界处腐蚀越严重,液面以下缺少氧气,腐蚀不严重,液面以上,缺少水,腐蚀也不严重,故C错误;D、该原电池放电时,正极上氢离子得电子发生还原反应形成氢气,Zn腐蚀速率增大,铜上放出气体的速率也增大,故D错误,答案选B。

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
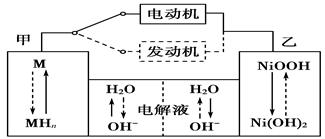
 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,甲电
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,甲电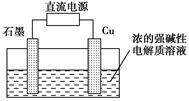
 Cu2O+H2↑,阴极的电极反应式是_____________________。
Cu2O+H2↑,阴极的电极反应式是_____________________。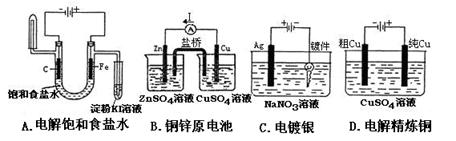

 2 H2O
2 H2O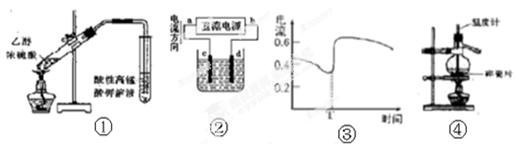
 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 (填答案编号)。
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 (填答案编号)。
