题目内容
【题目】通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
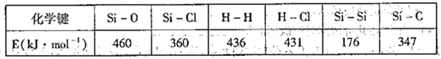
工业上高纯硅可通过下列反制取:SiCl4(g) +2H2(g)= Si(g) +4HCl(g),(已知 lmol晶体Si中2molSi -Si键),该反应产生的热量为
A. 吸收45kJ mo1-1 B. 放出412 kJ mo1-1
C. 吸收 236 kJ mo1-1 D. 放出236 kJ mo1-1
【答案】C
【解析】在晶体硅中由于1个Si可形成4个Si—Si键,每个Si原子对一个Si—Si键的贡献为![]() ,故在硅晶体中n(Si)︰n(Si—Si)=l︰(4×
,故在硅晶体中n(Si)︰n(Si—Si)=l︰(4×![]() )=1︰2。所以每生成1 mol Si,则形成2 mol Si—Si键,故有:△H =4×360 kJ·mol-1+2×436 kJ·mol-1-(2×176 kJ·mol-1+4×431 kJ·mol-1)=+236 kJ·mol-1,即吸收236 kJ mo1-1 ,答案选C。
)=1︰2。所以每生成1 mol Si,则形成2 mol Si—Si键,故有:△H =4×360 kJ·mol-1+2×436 kJ·mol-1-(2×176 kJ·mol-1+4×431 kJ·mol-1)=+236 kJ·mol-1,即吸收236 kJ mo1-1 ,答案选C。

【题目】A、B、C、D、E、F六种短周期元索,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如表所示:
化合物 | 甲 | 乙 | 丙 | 丁 |
化学式 | A2C | A2C2 | D2C2 | D2E |
回答下列问题:
(1)指出元素F在周期表中的位置___________。
(2)化合物丙的电子式为__________,用电子式表示形成化合物丁的过程_______。
(3) 向丁的溶液中加入硫酸酸化的乙溶液,写出相应的离子方程式:_______。
(4)固体氧化物燃料电池是以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许02-在其间通过,该电池的工作原理如图所示,其中多孔Pt电极a、b分别是气体C2、A2的载体。该电池的正极为______ (填a或b);02-流向______极(填“正”或“负”);该电池的负极反应为 _________ 。




