��Ŀ����
����Ŀ����ѧʵ�����������⻯ѧ֪ʶ���γɻ�ѧ������̽���봴��������������ѧ������
��1����ʵ��������Ũ������MnO2������ȡCl2���������ʵ�顣
�� ��ƽ���з���ʽ��
HCl(Ũ) + MnO2 ![]() MnCl2 + Cl2 + H2O___________
MnCl2 + Cl2 + H2O___________
�������ռ�Cl2����ȷװ����_______��
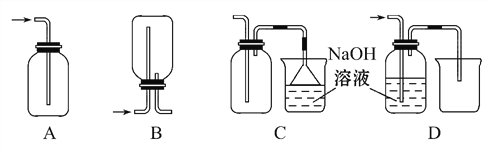
�� ��Cl2ͨ�뵽Ba(OH)2��Һ�з�����Ӧ�Ļ�ѧ����ʽΪ��______
�� ����������ȼ�յĻ�ѧ����ʽΪ��______________
�� ������������ˮ���뵽ʢ������NaHCO3��ĩ���Թ��У��ɿ��������У� ____
���𰸡� 4HCl(Ũ)+MnO2![]() MnCl2+Cl2��+2H2O C 2Ba(OH)2+2Cl2=BaCl2+Ba(ClO)2+2H2O 2Fe+3Cl2
MnCl2+Cl2��+2H2O C 2Ba(OH)2+2Cl2=BaCl2+Ba(ClO)2+2H2O 2Fe+3Cl2![]() FeCl3 ��ˮ��ɫ��dz����ɫ����ĩ�ܽ⣻�����ݲ���
FeCl3 ��ˮ��ɫ��dz����ɫ����ĩ�ܽ⣻�����ݲ���
����������1������Ԫ�ػ��ϼ۴ӣ�1�����ߵ�0�ۣ���Ԫ�ػ��ϼ۴�+4�۽��͵�+2�ۣ����Ը��ݵ��ӵ�ʧ�غ㡢ԭ���غ��֪����ʽΪ4HCl(Ũ)+MnO2![]() MnCl2+Cl2��+2H2O���������ܶȴ��ڿ�����������ˮ��Ӧ���������ſ������ռ�������Ϊ�����ж�����Ҫβ������������������������Һ���ն����������ͬʱҪע���ֹ��������ѡC���۽�Cl2ͨ�뵽Ba(OH)2��Һ�з�����Ӧ�Ļ�ѧ����ʽΪ2Ba(OH)2+2Cl2=BaCl2+Ba(ClO)2+2H2O��������������ȼ�յĻ�ѧ����ʽΪ2Fe+3Cl2
MnCl2+Cl2��+2H2O���������ܶȴ��ڿ�����������ˮ��Ӧ���������ſ������ռ�������Ϊ�����ж�����Ҫβ������������������������Һ���ն����������ͬʱҪע���ֹ��������ѡC���۽�Cl2ͨ�뵽Ba(OH)2��Һ�з�����Ӧ�Ļ�ѧ����ʽΪ2Ba(OH)2+2Cl2=BaCl2+Ba(ClO)2+2H2O��������������ȼ�յĻ�ѧ����ʽΪ2Fe+3Cl2![]() FeCl3����������ˮ��Ӧ���ɵ���������̼�����Ʒ�Ӧ�ų�������̼��������������ˮ���뵽ʢ������NaHCO3��ĩ���Թ��У��ɿ�����������ˮ��ɫ��dz����ɫ����ĩ���ܽ⣬�����ݲ�����
FeCl3����������ˮ��Ӧ���ɵ���������̼�����Ʒ�Ӧ�ų�������̼��������������ˮ���뵽ʢ������NaHCO3��ĩ���Թ��У��ɿ�����������ˮ��ɫ��dz����ɫ����ĩ���ܽ⣬�����ݲ�����

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�