题目内容
2.3g钠投入100g水中,下列叙述述错误的是
| A.钠浮在水面,熔化成银色光亮的小球 | B.钠贮存在煤油中 |
| C.所得溶液的质量分数为2.25﹪ | D.反应中转移0.1mol电子 |
C
解析试题分析:A、钠的密度小于水的熔点低,钠与水反应是放热反应,所以钠浮在水面,熔化成银色光亮的小球,A正确;B、钠是活泼的金属,极易被氧化,且极易与水反应,所以钠贮存在煤油中,B正确;C、2.3g钠的物质的量=2.3g÷23g/mol=0.1mol,投入100g水中,发生反应2Na+2H2O=2NaOH+H2↑,生成氢氧化钠0.1mol,质量是4.0g,氢气0.05mol,氢气质量是0.05mol×2=0.1g,所以所得溶液的质量分数为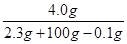 ×100%=3.91﹪,C不正确;D、钠在反应中失去1个电子,所以2.3g钠在反应中转移0.1mol电子,D正确,答案选C。
×100%=3.91﹪,C不正确;D、钠在反应中失去1个电子,所以2.3g钠在反应中转移0.1mol电子,D正确,答案选C。
考点:考查

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案为了测定某镁铝合金的成分,取14.7 g合金完全溶于500 mL 3 mol/L的硫酸中,再加入400 mL 8 mol/L的氢氧化钠溶液充分反应,最后只产生一种沉淀。则关于该合金的测定过程的描述正确的是( )
| A.合金中镁的质量分数为63.3%≤Mg%<100% |
| B.该合金中含有铝的质量至少为5.4 g |
| C.在产生沉淀后的溶液中一定含有0.2 mol NaAlO2 |
| D.在产生沉淀后的溶液中有1.5 mol Na2SO4 |
将含1 mol Na和1 mol Al的合金加入足量的水中,下列描述不正确的是 ( )
| A.金属Al无剩余 | B.c(Na+)=c(AlO-2) |
| C.生成气体为2 mol | D.c(Na+)=c(Al3+) |
在FeCl3和CuCl2混合液中,加入一定量的铁粉,充分反应后,溶液中的金属离子不可能是
| A.有Fe2+ | B.Cu2+、Fe2+ 和Fe3+ |
| C.仅有 Fe3+ 和Fe2+ | D.有Cu2+和Fe2+ |
1L某混合溶液中,溶质X、Y的浓度都为0.1mol?L﹣1,向混合溶液中滴加某溶液Z(0.1mol?L﹣1氢氧化钠或硫酸溶液)至溶液呈中性,所得沉淀的物质的量如图所示,则X、Y、Z分别是( )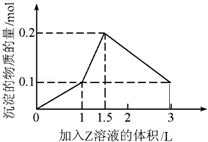
| A.氯化铝、氯化铁、氢氧化钠 | B.氯化铝、氯化镁、氢氧化钠 |
| C.偏铝酸钠、氢氧化钡、硫酸 | D.偏铝酸钠、氯化钡、硫酸 |
铁和铁合金是生活中常用的材料,下列说法正确的是
| A.一定条件下,铁粉可与水蒸气反应 | B.不锈钢是铁合金,只含金属元素 |
| C.铁与盐酸反应,铁合金不与盐酸反应 | D.在空气中,铁板比镀锌铁板更耐腐蚀 |
把生锈的铁钉放入足量稀盐酸中,可能发生的反应是( )
| A.只有置换反应 | B.只有复分解反应 |
| C.置换和复分解反应 | D.置换和分解反应 |
将26g CO和O2的混合气体充入一体积固定不变的密闭容器中(容器内有足量的Na2O2固体),此时容器的压强为p1,用电火花不间断地点燃,使其充分反应,恢复至原温度,结果固体增重14g,此时容器的压强为p2,则p1:p2为
| A.9:4 | B.7:3 | C.7:6 | D.6:7 |
下列物质既能与NaOH溶液反应,又能与盐酸反应的是
A.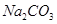 | B.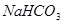 | C.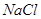 | D. |