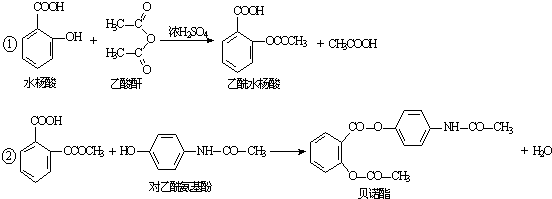
题目内容
已知X、Y、Z三种元素的原子核外具有相同的电子层数,且它们的最高价氧化物的水化物酸性依次增强,则下列判断正确的是( )
| A、原子半径按X、Y、Z的顺序增大 |
| B、阴离子的还原性按X、Y、Z顺序增强 |
| C、单质的氧化性按X、Y、Z顺序减弱 |
| D、氢化物的稳定性按X、Y、Z顺序增大 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z三种元素的原子核外具有相同的电子层数,则属于同一周期,且它们的最高价氧化物的水化物酸性依次增强,说明X、Y、Z三种元素的非金属性依次增强,其原子序数依次增大,再结合元素周期律解答.
解答:
解:X、Y、Z三种元素的原子核外具有相同的电子层数,则属于同一周期,且它们的最高价氧化物的水化物酸性依次增强,说明X、Y、Z三种元素的非金属性依次增强,其原子序数依次增大,
A.同一周期元素,其原子半径随着原子序数增大而减小,所以原子半径按X、Y、Z的顺序减小,故A错误;
B.元素的非金属性越强,其阴离子的还原性越强,非金属性X<Y<Z,所以阴离子的还原性按X、Y、Z顺序依次减弱,故B错误;
C.元素的非金属性越强,其单质的氧化性氧气,非金属性X<Y<Z,所以单质的氧化性按X、Y、Z顺序增强,故C错误;
D.元素的非金属性越强,其氢化物越稳定,非金属性X<Y<Z,氢化物的稳定性按X、Y、Z顺序增大,故D正确;
故选D.
A.同一周期元素,其原子半径随着原子序数增大而减小,所以原子半径按X、Y、Z的顺序减小,故A错误;
B.元素的非金属性越强,其阴离子的还原性越强,非金属性X<Y<Z,所以阴离子的还原性按X、Y、Z顺序依次减弱,故B错误;
C.元素的非金属性越强,其单质的氧化性氧气,非金属性X<Y<Z,所以单质的氧化性按X、Y、Z顺序增强,故C错误;
D.元素的非金属性越强,其氢化物越稳定,非金属性X<Y<Z,氢化物的稳定性按X、Y、Z顺序增大,故D正确;
故选D.
点评:本题考查了原子结构和元素周期律,明确“同一周期元素,元素非金属性强弱与其最高价氧化物的水化物酸性强弱的关系”是解本题关键,知道同一周期原子半径、阴离子的还原性、单质的氧化性、氢化物的稳定性的变化规律,题目难度不大.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
下列装置或操作能达到实验目的是( )
A、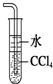 吸收NH3 |
B、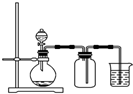 用铜片和稀硝酸制NO |
C、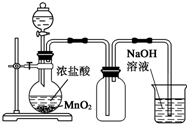 实验室制Cl2和尾气处理吸收 |
D、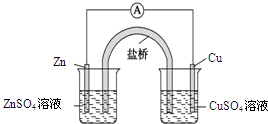 构成铜锌原电池(盐桥的作用:可使两烧杯的溶液联通) |
区别二氧化硫和二氧化氮气体最简捷的方法是( )
| A、观察颜色 |
| B、用干燥的品红试纸 |
| C、用湿润的无色酚酞试纸 |
| D、通入澄清石灰水 |
下列说法正确的是( )
| A、毛巾、口罩等个人用品要经常用开水蒸煮,被褥要放在太阳光下直射,其目的都是使病毒蛋白质变性 |
| B、用浓Na2SO4、CuSO4溶液或浓硝酸溶液使蛋清液发生盐析,进而分离、提纯蛋白质 |
| C、蛋白酶是蛋白质,它不仅可以催化蛋白质的水解反应,还可以催化淀粉的水解反应 |
| D、甘氨酸(H2N-CH2-COOH)既有酸性,又有碱性,是最简单的氨基酸 |
对于食品添加剂的论点中,合理的是( )
| A、绝大多数食品添加剂在过量使用时对人体有害,所以应禁止使用食品添加剂 |
| B、防腐剂能延长食品的保存期,减少食品的浪费和变质,所以应大量使用防腐剂 |
| C、食用新鲜食物比食用用防腐剂储存的作物有益,所以禁止使用防腐剂 |
| D、对于什么物质可作食品添加剂以及食品添加剂的用量,都应有严格的规定 |
已知下列反应热数据,有关分析或说法不正确的是( )
①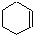 (g)+H2(g)→
(g)+H2(g)→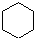 (g)△H=-119kJ?mol-1
(g)△H=-119kJ?mol-1
②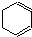 (g)+2H2(g)→
(g)+2H2(g)→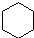 (g)△H=-237kJ?mol-1
(g)△H=-237kJ?mol-1
③ (g)+3H2(g)→
(g)+3H2(g)→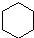 (g)△H=-208.4kJ?mol-1.
(g)△H=-208.4kJ?mol-1.
①
 (g)+H2(g)→
(g)+H2(g)→ (g)△H=-119kJ?mol-1
(g)△H=-119kJ?mol-1②
 (g)+2H2(g)→
(g)+2H2(g)→ (g)△H=-237kJ?mol-1
(g)△H=-237kJ?mol-1③
 (g)+3H2(g)→
(g)+3H2(g)→ (g)△H=-208.4kJ?mol-1.
(g)△H=-208.4kJ?mol-1.| A、上述四种有机物中环已烷最稳定 |
| B、苯分子中不存在独立的碳碳双键 |
| C、1,3-环已二烯比苯稳定 |
| D、苯与H2反应生成1,3-环已二烯吸收热量 |
把一小块镁、铝合金放入6mol?L-l的NaOH溶液中,可以形成微型原电池.则该电池负极上发生的电极反应为( )
| A、Mg-2e-═Mg2+ |
| B、A1+4OH--3e-═AlO2-+2H2O |
| C、4OH--4e-═2H2O+O2↑ |
| D、2H2O+2e-═2OH-+H2↑ |