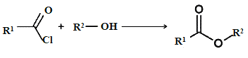题目内容
【题目】氯化氢(HCl),是无色而有刺激性气味的气体。对上呼吸道有强刺激,对眼、皮肤、黏膜有腐蚀。其水溶液俗称盐酸,学名氢氯酸。氯化氢极易溶于水,在0℃时,1体积的水大约能溶解500体积的氯化氢。实验室制取一般是用固体氯化钠和浓硫酸起反应,不加热或稍微加热,分别生成硫酸氢钠和氯化氢。 实验室可用如下装置制取氯化氢 ,化学方程式为:NaCl(s)+H2SO4=NaHSO4+HCl↑
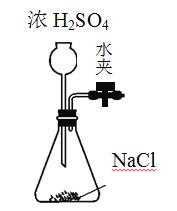
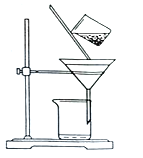
(1)如何检验该装置的气密性(请说明具体操作) _________。
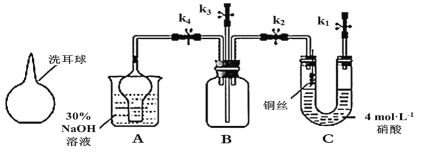
(2)多余的氯化氢如何处理?画出装置图。_________。
【答案】用水夹夹住导气管的橡胶管部分,从长颈漏斗向锥形瓶中注水,将长颈漏斗下口浸没,停止加水后,长颈漏斗中的液面高于锥形瓶中的液面,且液面差保持不变; 
【解析】
(1)利用液差法检查装置气密性;(2)根据氯化氢气体有毒又极易溶于水分析。
(1)利用液差法检查此装置的气密性,具体操作如下:用水夹夹住导气管的橡胶管部分,从长颈漏斗向锥形瓶中注水,将长颈漏斗下口浸没,停止加水后,长颈漏斗中的液面高于锥形瓶中的液面,一段时间后若液面差保持不变,则气密性良好;
(2)氯化氢气体有毒,如果不处理直接排放到空气中,会污染环境,用氢氧化钠溶液吸收多余的氯化氢,由于氯化氢易溶于水,容易倒吸,因此用如图所示的一个防倒吸尾气吸收装置 。
。

练习册系列答案
相关题目