题目内容
【题目】CO2是一种常用的化工原料。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。
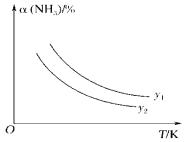
(1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示。该反应的ΔH________(填“>”、“<”或“=”,下同)0,若y表示压强,则y1________y2,若y表示反应开始时的n(NH3)/n(CO2),则y1________y2。
(2)T℃时,若向容积为2L的恒容密闭容器中加入3mol NH3和1mol CO2,达到平衡时,容器内压强为开始时的3/4。若保持条件不变,再向该容器中加入0.5mol CO2和1mol H2O,NH3的转化率将________(填“增大”、“减小”或“不变”)。
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为285.8kJ·mol-1、726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为_____。
(4)如图是某甲醇燃料电池工作的示意图。
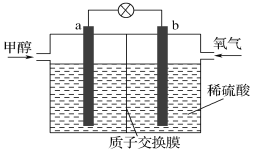
质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应为____,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为_____ g(假设反应物耗尽,忽略气体的溶解)。
(5)写出Na2CO3溶液中各离子浓度的大小关系__________________。
【答案】< > < 减小 CO2(g)+3H2(g)= CH3OH(l)+H2O(l) ΔH= -130.9kJ·mol1 CH3OH-6e-+H2O=CO2↑+6H+ 12 c(Na+)>c(CO32-)>c(OH- )>c(HCO3- )>c(H+ )
【解析】
Ⅰ.(1)结合温度和压强对平衡的影响分析;
(2)t℃时,若向容积为2L的密闭容器中加入3mol NH3和1mol CO2,达到平衡时,容器内压强为开始时的0.75倍,结合三行计算列式计算,气体压强之比等于气体物质的量之比,平衡常数K=![]() ,再向该容器中加入0.5mol CO2和1mol H2O,计算此时浓度商和平衡常数比较判断反应进行的方向;
,再向该容器中加入0.5mol CO2和1mol H2O,计算此时浓度商和平衡常数比较判断反应进行的方向;
Ⅱ、(3)氢气与甲醇的燃烧热分别为-285.8kJmol-1、-726.5kJmol-1,热化学方程式为:①H2(g)+![]() O2(g)=H2O(l) △H=-285.8kJmol-1;②CH3OH(l)+
O2(g)=H2O(l) △H=-285.8kJmol-1;②CH3OH(l)+![]() O2(g)=CO2(g)+2 H2O(l) △H= -726.5kJmol-1,盖斯定律计算①×3-②得到CO2与H2反应产生液态甲醇与液态水的热化学方程式;
O2(g)=CO2(g)+2 H2O(l) △H= -726.5kJmol-1,盖斯定律计算①×3-②得到CO2与H2反应产生液态甲醇与液态水的热化学方程式;
(4)负极反应式为CH3OH-6e-+H2O=CO2+6H+,正极反应式为O2+4H++4e-=2H2O,按照电极反应式计算;
(5)Na2CO3在溶液中存在两步水解,以第一步水解为主。
Ⅰ.(1)图象分析得到温度升高,氨气转化率减小说明平衡逆向进行,正反应为放热反应,压强越大平衡正向进行,氨气转化率增大,若y表示压强,则一定温度下y1大于y2,若y表示反应开始时的水碳比,升温平衡逆向进行,氨气转化率减小,一定温度下,水和二氧化碳之比越大,平衡逆向进行,氨气转化率越小,则y1小于y2;
(2)t℃时,若向容积为2L的密闭容器中加入3mol NH3和1mol CO2,达到平衡时,结合三行计算列式计算,设反应的二氧化碳为xmol,
2NH3(g)+CO2(g)CO(NH)2(s)+H2O(g)
起始量(mol) 3 1 0
变化量(mol) 2x x x
平衡量(mol)3-2x 1-x x
气体压强之比等于气体物质的量之比,容器内压强为开始时的0.75倍,3-2x+1-x+x=(3+1)×0.75,解得:x=0.5mol,此时K=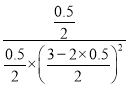 =1;
=1;
再向该容器中加入0.5mol CO2和1mol H2O,浓度商Qc=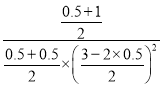 =1.5>K=1,平衡逆向进行,NH3的转化率将减小;
=1.5>K=1,平衡逆向进行,NH3的转化率将减小;
Ⅱ.(3)氢气与甲醇的燃烧热分别为-285.8kJmol-1、-726.5kJmol-1,热化学方程式为:①H2(g)+![]() O2(g)=H2O(l) △H=-285.8kJmol-1;②CH3OH(l)+
O2(g)=H2O(l) △H=-285.8kJmol-1;②CH3OH(l)+![]() O2(g)=CO2(g)+2 H2O(l) △H= -726.5kJmol-1,盖斯定律计算①×3-②得到CO2与H2反应产生液态甲醇与液态水的热化学方程式:CO2(g)+3H2(g)=CH3OH(l)+H2O(l) △H= -130.9 kJmol-1;
O2(g)=CO2(g)+2 H2O(l) △H= -726.5kJmol-1,盖斯定律计算①×3-②得到CO2与H2反应产生液态甲醇与液态水的热化学方程式:CO2(g)+3H2(g)=CH3OH(l)+H2O(l) △H= -130.9 kJmol-1;
(4)负极反应式为CH3OH-6e-+H2O=CO2+6H+,当转移1mol电子时,左侧质量减轻![]() ×12g=2g,还要有1mol H+通过质子交换膜进入右侧,质量减少1g,正极反应式为O2+4H++4e-=2H2O,右侧质量增加32g×
×12g=2g,还要有1mol H+通过质子交换膜进入右侧,质量减少1g,正极反应式为O2+4H++4e-=2H2O,右侧质量增加32g×![]() =8g,加上转移过来的1g H+,因此左右两侧溶液的质量之差为8g+1g+2g+1g=12g;
=8g,加上转移过来的1g H+,因此左右两侧溶液的质量之差为8g+1g+2g+1g=12g;
(5)Na2CO3在溶液中存在两步水解,以第一步水解为主,CO32-+H2OHCO3-+OH-,HCO3-+H2OH2CO3+OH-,则溶液中离子浓度大小的关系为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。

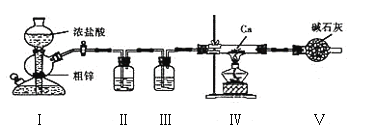
【题目】氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁。实验室制备装置和工业制备流程图如下:
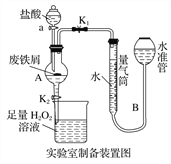
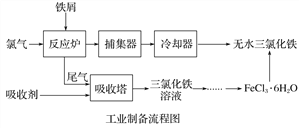
已知:(1)无水FeCl3的熔点为555 K、沸点为588 K。
(2)废铁屑中的杂质不与盐酸反应。
(3)不同温度下六水合氯化铁在水中的溶解度如下:
温度/℃ | 0 | 20 | 80 | 100 |
溶解度(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
实验室制备操作步骤如下:
Ⅰ.打开弹簧夹K1,关闭活塞K2,并打开活塞a,缓慢滴加盐酸;
Ⅱ.当……时,关闭弹簧夹K1,打开活塞K2,当A中溶液完全进入烧杯后关闭活塞a;
Ⅲ.将烧杯中溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(1)烧杯中足量的H2O2溶液的作用是_____________________________。
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是______________。
(3)从FeCl3溶液制得FeCl3·6H2O晶体的操作步骤是加入______________后__________________、过滤、洗涤、干燥。
(4)试写出吸收塔中反应的离子方程式:______________________。
(5)捕集器温度超过673 K时,存在相对分子质量为325的铁的氯化物,该物质的分子式(相对原子质量:Cl-35.5、Fe-56)为____________。
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100 mL溶液;取出10.00 mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol·L-1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32-=2I-+S4O62-)。
①滴定终点的现象是________________________________________________;
②样品中氯化铁的质量分数为__________________________。
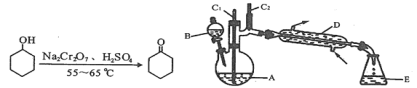
【题目】实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略)如下:
有关物质的物理性质见下表。
物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
水 | 100.0 | 1.0 |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为____________________________。
(2)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。
①滴加酸性Na2Cr2O7溶液的操作为_______________;
②蒸馏不能分离环己酮和水的原因是______________。
(3)环己酮的提纯需要经过以下一系列的操作:
a.往液体中加入NaCl固体至饱和,静置,分液;
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层;
c.加人无水MgSO4固体,除去有机物中少量的水;
d.过滤;
e.蒸馏、除去乙醚后,收集151~156℃馏分。
①B中水层用乙醚萃取的目的是_________;
②上述操作a、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有__,操作a中,加入NaC1固体的作用是____。
③恢复至室温时,分离得到纯产品体积为6mL,则环已酮的产率为_____。(计算结果精确到0.1%)
【题目】下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
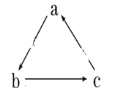
物质 | a | b | c |
A | Al2O3 | AlCl3 | Al(OH)3 |
B | NaAlO2 | Al(OH)3 | AlCl3 |
C | CO2 | NaHCO3 | Na2CO3 |
D | Na | Na2O | Na2O2 |
A.AB.BC.CD.D