题目内容
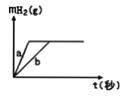
【题目】一定质量的钠、钾投入一定量的稀盐酸中,产生气体随时间变化的曲线如下图所示,则下列说法中正确的是
A. 投入的Na、K一定等质量
B. 投入的Na的质量大于K的质量
C. 曲线a为K,b为Na
D. 稀盐酸的量一定是不足量的
【答案】C
【解析】
A.通过方程式知,生成相同物质的量的氢气需要金属的质量不同,故A错误;B.有图象可知两种金属与盐酸反应生成氢气的量相等,则:
2Na+2HCl=2NaCl+H2↑,
46g 1mol
2K+2HCl=2KCl+H2↑,
78g 1mol,
所以生成相同量的氢气,消耗钾的质量多,故B错误;C.钾的金属性大于钠,则钾与酸反应速率大于钠与酸反应速率,即生成相同物质的量的氢气,钾需要的时间短,钠需要的时间长,所以曲线a为钾,b为钠,故C正确;D.因为钠、钾不仅和盐酸反应还和水反应,所以钠、钾生成相同物质的量的氢气与稀盐酸是否足量无关,故D错误;故选C。

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目