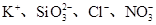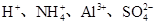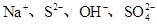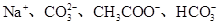题目内容
下列液体均处于25 ℃,有关叙述正确的是 ( )。
| A.某物质溶液的pH>7,则该物质一定是碱或强碱弱酸盐 |
| B.pH=6.5的牛奶中c(H+)是pH=4.5的H2SO4溶液中c(H+)的100倍 |
| C.pH=3的醋酸与pH=11的NaOH溶液等体积混合后溶液中:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.AgCl在等浓度的CaCl2溶液和NaCl溶液中的溶解度相同 |
C
本题考查了溶液中离子浓度的大小比较、溶解度等知识,意在考查考生对电解质溶液、电离与水解平衡等知识的理解能力。碱性溶液可能是碱、强碱弱酸盐的溶液,也可能是弱酸弱碱盐的溶液,A项错。pH是溶液中H+浓度的负对数,pH相差2个单位,c(H+)相差100倍,pH=4.5的H2SO4溶液中c(H+)是pH=6.5的牛奶中c(H+)的100倍,B项错。pH=3的醋酸溶液的物质的量浓度大于pH=11的NaOH溶液的物质的量浓度,两者等体积混合时醋酸过量,溶液呈酸性,溶液中各离子浓度关系正确,C正确;溶液中Cl-浓度影响AgCl的溶解度,等浓度的CaCl2溶液和NaCl溶液中Cl-浓度不同,AgCl的溶解度不同,D项错。

练习册系列答案
相关题目
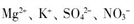
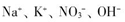
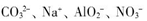
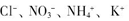
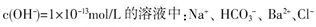


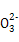 、OH- 6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是( )
、OH- 6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是( )