题目内容
(7分)(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
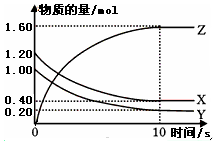
①此反应的化学方程式为________________;
②0~10s内,用Z表示的化学反应速率为________________;
③X的转化率为________________;
(2)恒温恒容时,某密闭容器中发生反应:C(s)+CO2(g) 2CO(g),下列描述中能说明该反应已达到化学平衡状态的是________________。
2CO(g),下列描述中能说明该反应已达到化学平衡状态的是________________。
①C(s)的浓度不再改变 ②CO2的体积分数不再改变
③气体的质量不再改变 ④气体的密度不再改变
⑤单位时间内消耗1molCO2,同时生成2molCO
⑥n(CO2):n(CO)=1:2 ⑦v正(CO2)=2v逆(CO)

①此反应的化学方程式为________________;
②0~10s内,用Z表示的化学反应速率为________________;
③X的转化率为________________;
(2)恒温恒容时,某密闭容器中发生反应:C(s)+CO2(g)
 2CO(g),下列描述中能说明该反应已达到化学平衡状态的是________________。
2CO(g),下列描述中能说明该反应已达到化学平衡状态的是________________。①C(s)的浓度不再改变 ②CO2的体积分数不再改变
③气体的质量不再改变 ④气体的密度不再改变
⑤单位时间内消耗1molCO2,同时生成2molCO
⑥n(CO2):n(CO)=1:2 ⑦v正(CO2)=2v逆(CO)
(1)①X(g)+Y(g) 2Z(g) (2分,不标状态也得分,“==”连接-1分)。
2Z(g) (2分,不标状态也得分,“==”连接-1分)。
②0.08mol/(L·s) (1分) ③66.7%或66.67% (2分) (2)②③④(2分)
 2Z(g) (2分,不标状态也得分,“==”连接-1分)。
2Z(g) (2分,不标状态也得分,“==”连接-1分)。②0.08mol/(L·s) (1分) ③66.7%或66.67% (2分) (2)②③④(2分)
试题分析:(1)①从图像中可以看出:(Ⅰ)X、Y两种物质的物质的量随时间变少,是反应物,Z的物质的量随时间变多,是生成物;(Ⅱ) 当反应进行到10秒后,X、Y、Z三种物质同时存在,说明这个反应是一个可逆反应;(Ⅲ) X、Y、Z三种物质物质的量的变化之比与化学方程式的化学计量系数之比相等,X的物质的量在10秒内变化了0.8mol,Y的物质的量在10秒内变化了0.8mol,Z的物质的量在10秒内变化了1.6mol,得到X(g)+Y(g)
 2Z(g);
2Z(g);②0~10s内,Z的物质量的变化为1.6mol,浓度的变化为1.6mol/2L="0.8" mol/L, Z的化学反应速率为0.8 mol/L/10s="0.08" mol/(L·s);
③X的转化率=0.8mol/1.2mol=66.7%。
(2)判断一个可逆反应是否达到化学平衡状态,可以从两个方面来考虑:(Ⅰ) v正=v逆>0;(Ⅱ) 混合物各成分浓度不变(注意固体的浓度时常数)。只要符合其一则达到平衡状态。②③④体现了混合物各成分浓度不变;⑤单位时间内消耗1molCO2,同时生成2molCO只说明了正反应速率,与逆反应的反应速率关系无法判断,不能判断是否达到化学平衡状态,错误;⑥中n(CO2)于n(CO)的关系不能判断各成分的浓度是否不变,不能判断是否达到化学平衡状态;⑦中2v正(CO2)=v逆(CO)才能说明v正=v逆,错误。

练习册系列答案
相关题目
 C+5D反应中,表示该反应速率最快的是( )
C+5D反应中,表示该反应速率最快的是( ) CO(g)+H2O(g) 反应过程中测定的部分数据见下表(表中t2>t1):
CO(g)+H2O(g) 反应过程中测定的部分数据见下表(表中t2>t1): Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是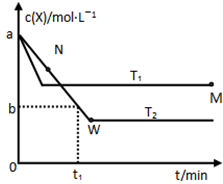
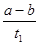 mol/(L·min)
mol/(L·min) O2NC6H4COO-+C2H5OH.两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。回答下列问题:
O2NC6H4COO-+C2H5OH.两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。回答下列问题: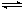 3Z(g) + W(s) ΔH>0 的叙述正确的是
3Z(g) + W(s) ΔH>0 的叙述正确的是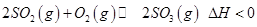 是制备硫酸的重要反应。下列说法正确的是
是制备硫酸的重要反应。下列说法正确的是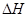 变大
变大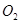
 3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是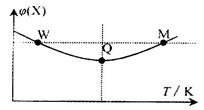
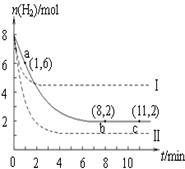
 CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是