题目内容
下列各组物质相互作用时,其中水既不作氧化剂,又不作还原剂,而反应仍属于氧化还原反应的是
| A.氟与水反应 | B.Na与水反应 | C.铝与强碱液作用 | D.过氧化钠与水反应 |
D
解析试题分析:反应前后存在元素化合价的变化是氧化还原反应的特征判断依据,水不做氧化剂与还原剂,需要水中氢元素和氧元素反应前后化合价不变,则A、氟与水反应2F2+2H2O=4HF+O2,水中氧元素化合价升高,作还原剂,故A不符合;B、Na与水反应2Na+2H2O2NaOH+H2↑,反应中水中氢元素化合价降低,作氧化剂,故B不符合;C、铝与强碱液作用,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,水中氢元素化合价降低,水做氧化剂,故C不符合;D、过氧化钠与水反应2Na2O2+2H2O=4NaOH+O2↑,是氧化还原反应,水中H和O元素化合价均不变,不是氧化剂也不是还原剂,过氧化钠既是氧化剂也是还原剂,故D符合,答案选D。
考点:考查水参与氧化还原反应的有关判断

汽车安全气囊是汽车安全性辅助配置之一。汽车剧烈碰撞时,安全气囊中发生反应:10NaN3 +2KNO3 ==K2O+5Na2O+16N2↑,则下列判断不正确的是
| A.NaN3是还原剂 |
| B.N2既是氧化产物又是还原产物 |
| C.氧化产物与还原产物物质的量之比为1:15 |
| D.标准状况下,当有10mol电子转移时生成358.4L N2 |
有关氧化还原反应的下列叙述正确的是
| A.氧化剂发生还原反应,还原剂发生氧化反应 |
| B.氧化剂被氧化,还原剂被还原 |
| C.在氧化还原反应中,氧化剂和还原剂一定是两种不同的物质 |
| D.氧化还原反应中,金属单质只作还原剂,非金属单质只作氧化剂 |
在一定条件下,RO3- 和氟气可发生如下反应:
RO3-+F2+2OH-=RO4-+2F-+H2O。从而可知在RO3-中,元素R的化合价是
| A.+4 | B.+5 | C.+6 | D.+7 |
铬是人体必需的微量元素,它与脂类代谢有密切联系,能增强人体内胆固醇的分解和排泄,但铬过量会引起污染,危害人类健康。不同价态的铬毒性不同,三价铬对人体几乎无毒,六价铬的毒性约为三价铬的100倍。下列叙述错误的是
| A.发生铬中毒时,可服用维生素C缓解毒性,因为维生素C具有还原性 |
| B.K2Cr2O7可以氧化乙醇,该反应可用于检查酒后驾驶 |
| C.在反应Cr2O72-+I-+H+→Cr3++I2+H2O中,氧化产物与还原产物的物质的量之比为3∶2 |
| D.污水中的Cr3+在溶解的氧气的作用下可被氧化为Cr2O72- |
某化学小组用下图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是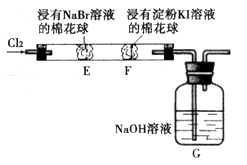
A.E处棉花球变成黄色,说明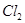 的氧化性比 的氧化性比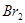 强 强 |
B.F处棉花球变成蓝色,说明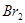 的氧化性比 的氧化性比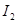 强 强 |
C.E处发生反应的离子方程式为: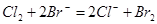 |
D.G装置中 溶液与 溶液与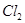 反应的离子方程式为: 反应的离子方程式为: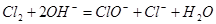 |
已知溶液中:还原性: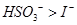 -氧化性
-氧化性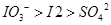 在含有3molNaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,则下列说法错误的是( )
在含有3molNaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,则下列说法错误的是( )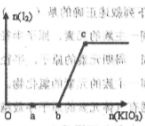
| A.a点时NaHSO3过量 |
| B.b点时还原产物为碘离子 |
| C.b点到c点,KIO3与NaHSO3反应生成单质碘 |
| D.加入的KIO3为0.4mol或1.12mol时,反应后溶液中碘离子均为0.4mol |
多硫化钠Na2Sx(x>2)在结构上与Na2O2、FeS2、CaC2等有相似之处。Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,反应中Na2Sx与NaClO的物质的量之比为1︰13,则x的值是
| A.5 | B.4 | C.3 | D.2 |
向某FeBr2溶液中,通入1.12L(标准状况)的Cl2,测得溶液中c(Br-)=3c(Cl-)=0.3mol/L。反应过程中溶液的体积变化不计。则下列说法中正确的是
| A.原溶液的浓度为0.1mol/L | B.反应后溶液中c(Fe3+)=0.1mol/L |
| C.反应后溶液中c(Fe3+)=c(Fe2+) | D.原溶液中c(Br-)=0.4mol/L |