题目内容
金星的大气中有一种称为硫化羰(COS)的分子,其结构与CO2类似,有关COS化学用语正确的是
A. | B.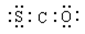 | C.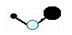 | D.O="C=S" |
D
试题分析:A.硫化羰(COS)的分子,其结构与CO2类似,为直线形分子,但氧原子和硫原子的半径不相等,故A错误;B.COS分子电子式为
 ,故B错误;C.硫化羰(COS)的分子,其结构与CO2类似,为直线形分子,不是V形分子,故C错误;D.二氧化碳是结构简式为O=C=O,所以硫化羰(COS)的分子的结构简式为O=C=S,故D正确;故选D。2的结构,硫化羰(COS)的分子的电子式、结构式、球棍模型、比例模型,培养了学生分析问题、运用知识解决问题的能力。
,故B错误;C.硫化羰(COS)的分子,其结构与CO2类似,为直线形分子,不是V形分子,故C错误;D.二氧化碳是结构简式为O=C=O,所以硫化羰(COS)的分子的结构简式为O=C=S,故D正确;故选D。2的结构,硫化羰(COS)的分子的电子式、结构式、球棍模型、比例模型,培养了学生分析问题、运用知识解决问题的能力。
练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
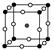

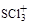 、SO2、SO32-、SO42-等。
、SO2、SO32-、SO42-等。