题目内容
3.按要求完成下列问题:(1)
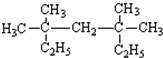 系统命名为:3,3,5,5-四甲基庚烷.
系统命名为:3,3,5,5-四甲基庚烷.(2)与H2加成生成
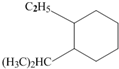 的炔烃的结构简式:
的炔烃的结构简式: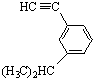 .
.(3)某烷烃分子中电子数为42,该烷烃的分子式为C5H12.
(4)现有五种有机物,请回答下列问题:
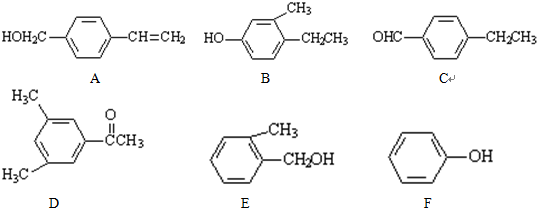
①A物质中含有的官能团名称为碳碳双键、羟基;
②D的一氯代物最多有4种;
③上述化合物中互为同分异构体的是A和C(填字母);互为同系物的是B和F(填字母).
分析 (1)烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上的碳原子进行编号;
(2)在有机物 的侧链碳架上添加碳碳三键就可以得到该炔烃的结构简式;
的侧链碳架上添加碳碳三键就可以得到该炔烃的结构简式;
(3)烷烃的通式为:CnH(2n+2),该有机物分子中含有电子数目为:6n+2n+2,据此计算出n;
(4)①根据有机物的结构写出分子中含有的官能团;
②根据氢原子的种类等于一氯代物的种类;
③同分异构体是分子式相同结构式不同的化合物;结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物,注意同系物中的“结构相似”是指物质种类相同,若含有官能团,官能团的种类与数目相同.
解答 解:(1)烷烃命名时,要选最长的碳链为主链,故主链上有7个碳原子,从离支链近的一端给主链上的碳原子进行编号,则在3号和5号碳上各有2个甲基,故名称为:
3,3,5,5-四甲基庚烷,故答案为:3,3,5,5-四甲基庚烷;
(2)与H2加成生成 ,在加成产物侧链上添加碳碳三键,只有一种添加方式,该炔烃的结构简式为:
,在加成产物侧链上添加碳碳三键,只有一种添加方式,该炔烃的结构简式为: ,
,
故答案为: ;
;
(3)烷烃的通式为:CnH(2n+2),碳原子含有6个电子,氢原子含有1个电子,则该有机物分子中含有的电子数为:6n+2n+2=42,解得n=5,该有机物分子式为:C5H12,故答案为:C5H12.
(4)①A物质中含有碳碳双键、醛基,故答案为:碳碳双键;醛基;
②D中含有4种氢原子,一氯代物有4种,故答案为:4;
③A和C的分子式相同,结构不同,互为同分异构体;B和F的结构相似,在分子组成上相差3个CH2原子团,互为同系物,故答案为:A和C;B和F.
点评 本题侧重有机物物官能团、分子式、等效氢以及物质的分类等考查,注重学生基础知识的掌握,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
13.下列反应既属于氧化还原反应,又属于吸热反应的是( )
| A. | 氢氧化钠与稀盐酸反应 | B. | 锌与稀硫酸反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 灼热的炭与二氧化碳反应 |
14.表中实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 向苯酚溶液中滴加稀溴水 | 观察白色沉淀三溴苯酚 |
| B | 向待测液中加入碳酸钠溶液 | 鉴别乙酸、乙酸乙酯、乙醇 |
| C | 向3ml5%CuSO4溶液中滴加3-4滴2%氢氧化钠溶液,再向其中加入0.5ml乙醛,加热 | 检验醛基 |
| D | 将溴乙烷与氢氧化钠溶液共热,冷却,继续滴加硝酸银溶液 | 检验溴乙烷中的溴元素 |
| A. | A | B. | B | C. | C | D. | D |
8.下列说法或计算正确的是( )
| A. | 采用加热蒸发溶剂的方法可以使浓度为4 mol/L的盐酸溶液的浓度变为8 mol/L | |
| B. | 把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10% | |
| C. | 将2.3 g Na投入到97.7g水中充分反应,所得溶液的质量分数为4.0% | |
| D. | 已知某温度下KNO3的溶解度是31.6 g,该温度下将20 g KNO3溶解于50 g水中,充分溶解,获得溶液的质量分数是28.6% |
12.下列说法正确的是( )
| A. | π键是由两个p轨道“头碰头”重叠形成的 | |
| B. | σ键一定是有s轨道参与形成的 | |
| C. | 甲烷分子中的键全为σ键而乙烯分子中含σ键和π键 | |
| D. | H2分子中含σ键而Cl2分子中还含π键 |
13.某小组要探究卤族元素的非金属性强弱,设计了如下实验,请按要求填空.
| 实验 | 现象 | 离子方程式 |
| 1.将少量氯水分别加入盛有NaBr溶液(试管①)和KI溶液(试管②)中,用力振荡后加入少量四氯化碳,振荡,静置 | 写出试管②中的实验现象 溶液分层下层为紫红色 | 写出试管①中的离子方程式: Cl2+2Br-=2Cl-+Br2 |
| 2.将少量溴水加入盛有KI溶液(试管③)中,用力振荡后加入少量四氯化碳,振荡,静置 | 现象略 | 写出试管③中的离子方程式: Br2+2I-=2Br-+I2 |
| 实验结论: 元素非金属性由强到弱的顺序为:Cl>Br>I. | ||
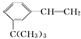 有如下性质:
有如下性质: .
.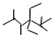 的名称是2,2,4,5-四甲基-3,3-二乙基庚烷,
的名称是2,2,4,5-四甲基-3,3-二乙基庚烷,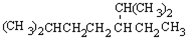 的名称为2,6-二甲基-3-乙基庚烷.
的名称为2,6-二甲基-3-乙基庚烷.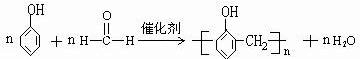 ,
,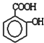 )滴入Na2CO3溶液中发生的化学方程式:
)滴入Na2CO3溶液中发生的化学方程式: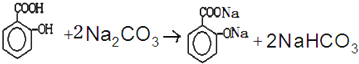 ,
,