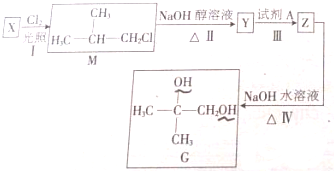
籾朕坪否
14⤴0.1mol•L-1議和双叱嶽卑匣⇧凪pH喇寄欺弌議乏會電双屎鳩議頁↙ ⇄〙Na2CO3 〖CH3COONa 〗NaCl ∠NaHCO3 ⊥NH4Cl⤴
| A⤴ | ∠﹅〙﹅〖﹅〗﹅⊥ | B⤴ | 〖﹅〙﹅∠﹅〗﹅⊥ | C⤴ | 〗﹅〙﹅∠﹅〖﹅⊥ | D⤴ | 〙﹅∠﹅〖﹅〗﹅⊥ |
蛍裂 功象卑匣議磨珠來參式旋喘冦窃議邦盾殻業栖鳩協卑匣嶄pH寄弌⇧磨議磨來埆樋夸磨議磨功宣徨邦盾殻業埆寄⇧凪屢揖敵業墜冦卑匣議pH埆寄⤴
盾基 盾⦿〙娘磨墜卑匣格珠來⇧pH﹅7⇧屢揖敵業議娘磨墜才閑磨墜⇧娘磨墜議pH寄噐閑磨墜◉
〖閑磨墜頁膿珠樋磨冦⇧凪卑匣格珠來⇧pH﹅7◉
〗柁晒墜頁膿磨膿珠冦⇧凪卑匣格嶄來⇧pH=7◉
∠娘磨狽墜頁膿珠樋磨磨塀冦⇧娘磨狽功宣徨邦盾殻業寄噐窮宣殻業⇧擬崑凪卑匣格珠來來⇧pH﹅7⇧嚥屢揖敵業議娘磨墜才閑磨墜卑匣曳熟⇧卑匣PH娘磨墜寄噐娘磨狽墜寄噐閑磨墜◉
⊥柁晒錻頁膿磨樋珠冦⇧錻功宣徨邦盾遇聞凪卑匣格樋磨來⇧pH〽7◉
侭參宸叱嶽卑匣pH寄弌乏會頁〙﹅∠﹅〖﹅〗﹅⊥⇧
絞僉D⤴
泣得 云籾深臥阻pH寄弌議登僅⇧枠功象卑匣議磨珠來寄悶蛍窃⇧壅功象樋宣徨議邦盾敵業登僅pH寄弌⇧廣吭娘磨狽功宣徨壓邦卑匣戦窮宣圭塀音揖⇧籾朕佃業嶄吉⤴

膳楼過狼双基宛
屢購籾朕
4⤴和双傍隈嶄屎鳩議頁↙ ⇄
| A⤴ | 厰路嶄娘娘褒囚議囚嬬頁厰莱嶄娘娘汽囚議囚嬬議2蔚 | |
| B⤴ | NH4+嶄4倖N-H囚議囚嬬音屢揖 | |
| C⤴ | N-O囚議自來曳C-O囚議自來弌 | |
| D⤴ | 白漉庁侏  燕幣屈剳晒娘蛍徨⇧匆辛參燕幣屈剳晒紀蛍徨 燕幣屈剳晒娘蛍徨⇧匆辛參燕幣屈剳晒紀蛍徨 |
5⤴和双光夕侭幣議賑畜來殊臥嶄⇧嬬傍苧廾崔息賑議頁↙ ⇄
| A⤴ | 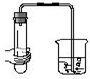 | B⤴ | 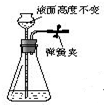 | C⤴ |  | D⤴ | 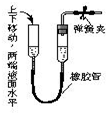 |
2⤴玉巓豚圷殆宣徨aA2+、bB+、cC3+、dD- 脅醤嗤屢揖窮徨蚊潤更⇧夸和双偃峰屎鳩議頁↙ ⇄
| A⤴ | 圻徨磯抄B﹅A﹅D | B⤴ | 宣徨磯抄C﹅D﹅B﹅A | ||
| C⤴ | 汽嵎珊圻來A﹅B﹅D﹅C | D⤴ | A、B、C、D辛嬬頁及屈巓豚圷殆 |
19⤴厮岑晒僥郡哘2C↙s⇄+O2↙g⇄?2CO↙g⇄◉2CO↙g⇄+O2↙g⇄?2CO2↙g⇄脅頁慧犯郡哘⤴象緩容僅⇧和双傍隈音屎鳩議頁↙凪万訳周屢揖⇄↙ ⇄
| A⤴ | 56g CO才32g O2侭醤嗤議悳嬬楚寄噐88g CO2侭醤嗤議悳嬬楚 | |
| B⤴ | CO音泌 CO2糧協 | |
| C⤴ | 12g C侭醤嗤議嬬楚匯協互噐28g CO侭醤嗤議嬬楚 | |
| D⤴ | 繍匯協嵎楚議命伴付⇧伏撹CO2曳伏撹CO扮慧竃議犯楚謹 |
6⤴葎阻决海邦惚議隠亙豚⇧和双議邦惚贋慧圭隈恷栽癖議頁↙ ⇄
| A⤴ | 慧秘絵笥議否匂嶄 | |
| B⤴ | 慧秘償倒狛互談磨蛇卑匣壕輿議畜撃否匂嶄 | |
| C⤴ | 慧秘畜撃議否匂嶄 | |
| D⤴ | 慧秘割嗤富楚厰路議畜撃否匂嶄 |
3⤴厮岑路癒壓匯協訳周和辛參窟伏泌和郡哘⦿2RCH=CHR>★RCH=CHR+R>CH=CHR>↙R、R>脅燕幣癒児⇄
乎郡哘各葎路癒鹸蛍盾郡哘⇧2005定典唄櫛晒僥襲祥娩嚠冩梢乎郡哘議叱了親僥社⤴和双斤乎郡哘字尖議佳霞刃協音屎鳩議頁↙ ⇄
乎郡哘各葎路癒鹸蛍盾郡哘⇧2005定典唄櫛晒僥襲祥娩嚠冩梢乎郡哘議叱了親僥社⤴和双斤乎郡哘字尖議佳霞刃協音屎鳩議頁↙ ⇄
| A⤴ | 郡哘麗蛍徨脅僅叢C=C囚 | |
| B⤴ | 郡哘麗蛍徨脅僅叢R-C囚 | |
| C⤴ | 郡哘麗蛍徨脅僅叢R>-C囚 | |
| D⤴ | 曾蛍徨郡哘麗嶄⇧匯倖僅叢R-C囚⇧総匯倖僅叢R>-C囚 |
4⤴卆象和双糞刮孖嵆⇧誼竃議潤胎屎鳩議頁↙ ⇄
| 荷恬 | 糞刮孖嵆 | 潤胎 | |
| A | 﨑NaBr卑匣嶄紗秘柁邦⇧壅紗秘牛頚KI卑匣 | 卑匣延清 | 剳晒來⦿Cl2﹅Br2﹅I2 |
| B | 繍汰頭慧秘冦磨嶄 | 恢伏賑倒議堀楕蝕兵熟蛸⇧昧朔紗酔⇧朔栖嗽幟愁受蛸 | H+議敵業頁唹峒郡哘堀楕議率匯咀殆 |
| C | 﨑宦滅卑匣嶄紗秘蓮葬磨⇧邦圈紗犯朔⇧紗秘仟崙狽剳晒有⇧紗犯 | 誼欺清弼卑匣 | 宦滅邦盾恢麗短嗤珊圻來 |
| D | 﨑働易頚嶄砧秘蓮葬磨⇧繍伏撹議賑悶宥秘瞳碕卑匣 | 瞳碕卑匣擁弼 | 賑悶嶄根嗤Cl2 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |