题目内容
(1)下列实验操作或对实验事实的描述不正确的是 (填序号)。
A.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
B.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大
C.分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出
D.用托盘天平称量11.74g氯化钠晶体
E.用结晶法分离硝酸钾和氯化钠的混合物
(2)实验室需要0.1 mol·L-1NaOH溶液450 moL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
①如图所示的仪器中配制溶液肯定不需要的是 (填序号);配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。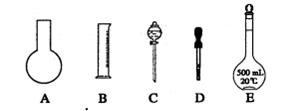
②下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
③请计算需用托盘天平称取固体NaOH的质量为 g。某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧杯的实际质量为 g。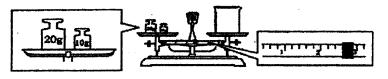
④根据计算得知,所需质量分数为98%、密度为I.84 g·cm-3的浓硫酸的体积为 mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是 。
(1)D (2)①A C; 烧杯、玻璃棒 ②B C E ③ 2.0;27.4
④13.6; 将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌。
解析试题分析:(1)瓷坩埚含有二氧化硅,能与碱性物质反应,故A项正确;定容时俯视溶液的体积偏小,使浓度偏大,B项正确;为了彻底分离互不混溶的液体,当下层液体流尽时,立即关闭旋塞,然后再从漏斗上口把上层液体倾倒出来,C项正确;托盘天平的读数为小数点后一位,D项错误;硝酸钾的溶解度随温度变化大,氯化钠溶解度随温度变化小,可用结晶法分离。
(2)①配制溶液不用烧瓶和分液漏斗,要用烧杯和玻璃杯;
②容量瓶不能贮存溶液,也不能用来加热,另外容量瓶只有一条刻度线,不能测量规格以下的液体的体积;
③根据容量瓶的规格,需配制500ml溶液,m(NaOH)=0.5L×0.1mol/L×40g/mol=2g;图中所示,物质和砝码位置放反了,烧杯的质量为30g-2.6g=27.4g;
④0.5L×0.5mol?L?1=V×1.84g?cm?3×98%,可得V=13.6ml。
考点:本题考察化学实验基本操作和化学计算。

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
| A.甲装置:可用来证明碳的非金属性比硅强 |
| B.乙装置:橡皮管的作用是能使水顺利流下 |
| C.丙装置:用图示的方法不能检查此装置的气密性 |
| D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
下列有关实验装置进行的相应实验,能达到实验目的的是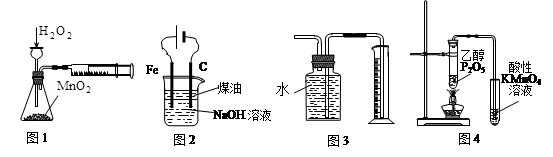
| A.图1定量测定H2O2的分解速率 |
| B.图2装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.图3装置测量Cu与浓硝酸反应产生气体的体积 |
| D.图4证明CH3CH2OH发生消去反应生成了乙烯 |
下列仪器不能加热的是
| A.烧瓶 | B.烧杯 | C.蒸发皿 | D.容量瓶 |
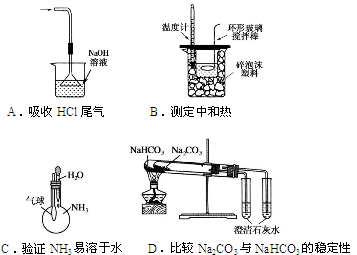
“封管试验”具有简易、方便、节约、绿色等优点。观察下列四个“封管试验”(夹持装置未画出),判断下列说法正确的是
| A.加热时,a上部聚集了固体NH4Cl,说明NH4C1的热稳性比较好 |
| B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体 |
| C.加热时,c中溶液红色变深,冷却后又变浅 |
| D.水浴时,d内气体颜色变浅,e内气体颜色加深 |




 8Na2CrO4+2 Fe2O3+8CO2↑;
8Na2CrO4+2 Fe2O3+8CO2↑; 2CrO42-+2H+
2CrO42-+2H+