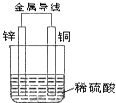
��Ŀ����
����Ŀ���Թ�����Ϊ�����������������V2O5���ǽӴ�����������Ĵ������ӷϷ������л���V2O5�ȱ�����Ⱦ����
����������Դ�ۺ����ã��Ϸ���������Ҫ�ɷ�Ϊ��
���� | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
��������/% | 2.2��2.9 | 2.8��3.1 | 22��28 | 60��65 | 1��2 | ��1 |
������һ�ַϷ��������չ���·�ߣ�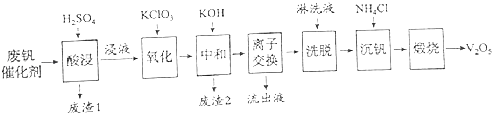
�ش��������⣺
��1���������ʱV2O5ת��ΪVO2+ �� ��Ӧ�����ӷ���ʽΪ �� ͬʱV2O4ת��VO2+ �� ������1������Ҫ�ɷ��� ��
��2��������������ʹ3 mol��VO2+��ΪVO2+ �� ����Ҫ������KClO3����Ϊmol��
��3�����к͡�����֮һ��ʹ����V4O124����ʽ��������Һ�У�������2���к��� ��
��4�������ӽ������͡�ϴ�ѡ��ɼ�ʾΪ��4ROH+V4O124��![]() R4V4O12+4OH������ROHΪǿ���������ӽ�����֬����Ϊ�����ϴ��Ч�ʣ���ϴҺӦ�ó��ԣ���ᡱ������С�����
R4V4O12+4OH������ROHΪǿ���������ӽ�����֬����Ϊ�����ϴ��Ч�ʣ���ϴҺӦ�ó��ԣ���ᡱ������С�����
��5��������Һ���������������� ��
��6�����������õ�ƫ����泥�NH4VO3��������д�������ա��з�����Ӧ�Ļ�ѧ����ʽ ��
���𰸡�
��1��V2O5+2H+=2VO2++H2O��SiO2
��2��0.5
��3��Fe��OH��3��Al��OH��3
��4����
��5��K+
��6��2NH4VO3![]() V2O5+H2O+2NH3��
V2O5+H2O+2NH3��
���������ӷϷ������л���V2O5 �� �����̿�֪���������ʱV2O5ת��ΪVO2+ �� V2O4ת��VO2+ �� ����������������ת��Ϊ���������ӣ�ֻ��SiO2���ܣ�����˵õ�������1ΪSiO2 �� Ȼ���������KClO3 �� ��VO2+��ΪVO2+ �� �ټ�KOHʱ�������ӡ�������ת��ΪFe��OH��3��Al��OH��3������ͬʱ�к����ᣬ���˵õ�������2ΪFe��OH��3��Al��OH��3 �� �����ӽ������͡�ϴ�ѡ��ɼ�ʾΪ��4ROH+V4O124��![]() R4V4O12+4OH�� �� ��ROHΪǿ���������ӽ�����֬��֪���������������÷�Ӧ�����ƶ�������Һ����ҪΪ����أ����������õ�ƫ����泥�NH4VO3�������������ա�ʱ�ֽ�����V2O5 ��
R4V4O12+4OH�� �� ��ROHΪǿ���������ӽ�����֬��֪���������������÷�Ӧ�����ƶ�������Һ����ҪΪ����أ����������õ�ƫ����泥�NH4VO3�������������ա�ʱ�ֽ�����V2O5 ��
��1���������ʱV2O5ת��ΪVO2+ �� ��Ӧ�����ӷ���ʽΪV2O5+2H+=2VO2++H2O��������������֪����1ΪSiO2 �� ���Դ��ǣ�V2O5+2H+=2VO2++H2O��SiO2��
��2��3 mol��VO2+��ΪVO2+ �� ʧȥ3 mol���ӣ�1molKClO3ת����KCl�õ�6 mol���ӡ��ɵ����غ��֪������Ҫ������KClO3����Ϊ0.5mol�����Դ��ǣ�0.5��
��3������������������֪����2ΪFe��OH��3��Al��OH��3 �� ���Դ��ǣ�Fe��OH��3��Al��OH��3��
��4������ǿ���������ӽ�����֬�ɡ����ӽ������͡�ϴ�ѡ�����Ӧѡ�����������ʹ�ã���OH��Ũ�ȴ�Ӧ�����ƶ����ϴ��Ч�ʣ����Դ��ǣ����5��������������֪������Һ����ҪΪ����أ�������Һ����������������K+ �� ���Դ��ǣ�K+��
��6�������ա��з�����Ӧ�Ļ�ѧ����ʽΪ2NH4VO3![]() V2O5+H2O+2NH3�������Դ��ǣ�2NH4VO3
V2O5+H2O+2NH3�������Դ��ǣ�2NH4VO3![]() V2O5+H2O+2NH3����
V2O5+H2O+2NH3����

 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�����Ŀ��������ͼװ�òⶨ�к��ȵ�ʵ�鲽�����£� ����ȡ50mL 0.25mol/L H2SO4��Һ����С�ձ��У������¶ȣ�
����ȡ50mL 0.55mol/L NaOH��Һ�������¶ȣ�
�۽�NaOH��Һ����С�ձ��У���Ͼ��Ⱥ�������Һ�¶ȣ���ش�
��1����ͼ��ʾ������A���������� 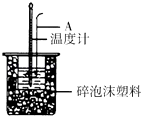
��2��NaOH��Һ�Թ�����ԭ�� ��
��3������NaOH��Һ����ȷ������������ĸ����
A.�ز�������������
B.һ��Ѹ�ټ���
C.�������
��4��ʹ������NaOH��Һ��Ͼ��ȵ���ȷ������ ��
��5������Һ���ܶȾ�Ϊ1gcm��3 �� �кͺ���Һ�ı�����c=4.18J��g�棩��1 �� �����ʵ������д�����к��ȵ��Ȼ�ѧ����ʽ
�¶� | ��ʼ�¶�t1/�� | ��ֹ�¶� | �¶Ȳ�ƽ��ֵ | ||
H2SO4 | NaOH | ƽ��ֵ | |||
1 | 25.0 | 25.2 | 28.5 | ||
2 | 24.9 | 25.1 | 28.3 | ||
3 | 25.5 | 26.5 | 31.8 | ||
4 | 25.6 | 25.4 | 29.0 | ||
��6������ʵ����ֵ�����57.3kJ/mol��ƫ�����ƫ���ԭ������ǣ�����ĸ�� a��ʵ��װ�ñ��¡�����Ч����
b���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
c�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
��7����������ȷ����ȡ���Һ������¶ȣ� ��
����Ŀ������ˮ�м����������ʣ����и������ȷ���ǣ� ��
ѡ�� | �������� | ���� | ���ͻ����ӷ���ʽ |
A | AgNO3��Һ | �а�ɫ�������� | Cl��+Ag+�TAgCl�� |
B | ʯ����Һ | �Ժ�ɫ | ��ˮ�������ᡢ������ |
C | CaCO3 | ������ų� | CO |
D | FeCl2��KSCN��Һ | �к�ɫ�������� | 2Fe2++Cl2�T2Fe3++2Cl�� |
A.A
B.B
C.C
D.D
����Ŀ���о�̼���仯������ת������Դ�ij�����á���̼����������Ҫ�����ã�
��1����֪����CH4��g��+H2O��g��CO��g��+3H2��g����H1=+206.1kJmol��1
��2H2��g��+CO��g��CH3OH��l����H2=��128.3kJmol��1
��2H2��g��+O2��g��2H2O ��g����H3=��483.6kJmol��1
25��ʱ���ں��ʵĴ��������£����ü��������һ���ϳ�Һ̬�״����Ȼ�ѧ����ʽΪ ��
��2�����÷�Ӧ�����Ʊ�������Ϊ��̽���¶ȡ�ѹǿ�Է�Ӧ�����ʡ�ת���ʵ�Ӱ�죬ijͬѧ�������������Ա�ʵ�飨�¶�Ϊ400���500�棬ѹǿΪ101kPa��404kPa����
ʵ����� | �¶ȡ� | ѹǿ/kPa | CH4��ʼŨ��/molL��1 | H2O��ʼŨ��/molL��1 |
1 | 400 | p | 3.0 | 7.0 |
2 | t | 101 | 3.0 | 7.0 |
3 | 400 | 101 | 3.0 | 7.0 |
��ʵ��2��ʵ��3��ȣ���ƽ�ⳣ����ϵ��K2K3�����������������=������
�ڽ������ʵ�����CH4��ˮ��������1L�����ܱ������У�����������Ӧ����400���´ﵽƽ�⣬ƽ�ⳣ��K=27����ʱ������CO���ʵ���Ϊ0.10mol����CH4��ת����Ϊ ��
��3����ѧ�������CO2�� ȡ C��̫���ܹ�����ͼ1��ʾ��
�١�����ϵͳ�������ķ�Ӧ��n��FeO����n��CO2��=6��1����Fe xOy�Ļ�ѧʽΪ ��
�ڡ��ȷֽ�ϵͳ����ÿ�ֽ�l mol Fe xOy �� ת�Ƶ��ӵ����ʵ���Ϊ �� 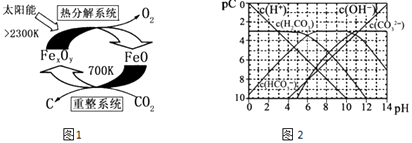
��4��pC����pH����ָ��ϡ��Һ�е�����Ũ�ȵij��ø�����ֵ����ij��Һ�����ʵ�Ũ��Ϊ1��10��3molL��1 �� �����Һ�����ʵ�pC=��lg��1��10��3��=3����ͼ2Ϊ25��ʱH2CO3��Һ��pC��pHͼ����ش��������� ��������Ũ��С��10��5mol/L������Ϊ�����Ӳ����ڣ���
����ͬһ��Һ�У�H2CO3��HCO3����CO32������ܡ����ܡ����������森
����H2CO3һ������ƽ�ⳣ������ֵKa1= ��
������ѪҺ����Ҫͨ��̼�����λ�����ϵ ![]() ���Ե����������ά��pH=7.4���������������ѪҺ��ʱ��ѪҺ������ϵ�е�
���Ե����������ά��pH=7.4���������������ѪҺ��ʱ��ѪҺ������ϵ�е� ![]() ���ս� ��
���ս� ��
A�����B����СC����������D�����жϣ�