题目内容
(5分)在固定容积的密闭容器中,有可逆反应nA(g)+mB(g)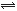 pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值 ,混合气体的密度 ;降温时,混合气体的平均相对分子质量 ;加入催化剂,气体的总物质的量 ;充入C,则A、B的物质的量 。(填增大、减小、不变、不确定)
pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值 ,混合气体的密度 ;降温时,混合气体的平均相对分子质量 ;加入催化剂,气体的总物质的量 ;充入C,则A、B的物质的量 。(填增大、减小、不变、不确定)
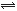 pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值 ,混合气体的密度 ;降温时,混合气体的平均相对分子质量 ;加入催化剂,气体的总物质的量 ;充入C,则A、B的物质的量 。(填增大、减小、不变、不确定)
pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值 ,混合气体的密度 ;降温时,混合气体的平均相对分子质量 ;加入催化剂,气体的总物质的量 ;充入C,则A、B的物质的量 。(填增大、减小、不变、不确定)减小;不变;减小;不变;增大
试题分析:由于该反应的正反应是吸热反应,所以根据平衡移动原理:升高温度,平衡向正反应方向移动,c(B)减小,c(C)增大,所以c(B)/c(C)减小;因为反应前后气体的质量不变,容器的容积也不变,所以混合气体的密度不变;降温时,平衡向放热反应方向移动,即向逆反应方向移动,由于该反应的正反应是气体体积减小的反应,所以平衡逆向移动,气体的物质的量增大,而气体的质量不变,所以混合气体的平均相对分子质量减小;加入催化剂,平衡不发生移动,气体的总物质的量不变;充入C,会发生反应产生A、B两种物质,则A、B的物质的量增大;

练习册系列答案
相关题目
 3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是
3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是 HBr+HBrO,下列措施,不能使溶液颜色变浅的是
HBr+HBrO,下列措施,不能使溶液颜色变浅的是 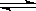 2Z2在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是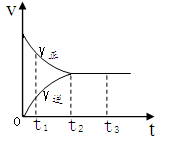
 2C(气)达到平衡的标志是( )
2C(气)达到平衡的标志是( ) 
 a Z(g)。
a Z(g)。