题目内容
1.肉桂酸是一种香料,具有很好的保香作用,通常作为配香原料,可使主香料的香气更加清香.实验室制备肉桂酸的化学方程式为: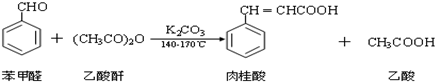
主要试剂及其物理性质
| 名称 | 分子量 | 性状 | 密度g/cm3 | 熔点℃ | 沸点℃ | 溶解度:克/100ml溶剂 | ||
| 水 | 醇 | 醚 | ||||||
| 苯甲醛 | 106 | 无色液体 | 1.06 | -26 | 178-179 | 0.3 | 互溶 | 互溶 |
| 乙酸酐 | 102 | 无色液体 | 1.082 | -73 | 138-140 | 12 | 溶 | 不溶 |
| 肉桂酸 | 148 | 无色结晶 | 1.248 | 133-134 | 300 | 0.04 | 24 | 溶 |
Ⅰ.合成:按图1连接仪器,加入5.3g苯甲醛、10.2g乙酸酐和7.02g无水碳酸钾.在140~170℃,将此混合物回流45min.
Ⅱ.分离与提纯:①将上述合成的产品冷却后边搅拌边加入40ml水浸泡5分钟,并用水蒸气蒸馏,从混合物中除去未反应的苯甲醛,得到粗产品;②将上述粗产品冷却后加入40ml 10%的氢氧化钠水溶液,再加90ml水,加热活性炭脱色,趁热过滤、冷却;③将1:1的盐酸在搅拌下加入到肉桂酸盐溶液中,至溶液呈酸性,经冷却、减压过滤、洗涤、干燥等操作得到较纯净的肉桂酸;
水蒸气蒸馏:使有机物可在较低的温度下从混合物中蒸馏出来,可以避免在常压下蒸馏时所造成的损失,提高分离提纯的效率.同时在操作和装置方面也较减压蒸馏简便一些,所以水蒸气蒸馏可以应用于分离和提纯有机物.回答下列问题:
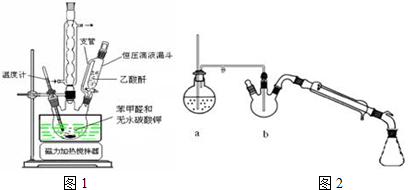
(1)合成肉桂酸的实验需在无水条件下进行,实验前仪器必须干燥的原因是乙酸酐易水解.实验中为控制温度在140~170℃需在BD中加热.
A.水 B.甘油(沸点290℃) C.砂子 D.植物油(沸点230~325℃)
(2)图2中装置a的作用是产生水蒸气,装置b中长玻璃导管要伸入混合物中的原因是使混合物与水蒸气充分接触,有利于提纯肉桂酸,水蒸气蒸馏后产品在三颈烧瓶(填仪器名称);
(3)趁热过滤的目的防止肉桂酸钠结晶而析出堵塞漏斗;
(4)加入1:1的盐酸的目的是使肉桂酸盐转化为肉桂酸,析出肉桂酸晶体过滤后洗涤,洗涤剂是水;
(5)5.3g苯甲醛、10.2乙酸酐和7.02g无水碳酸钾充分反应得到肉桂酸实际3.1g,则产率是41.9%(保留3位有效数字).
分析 (1)乙酸酐易水解,所以仪器必须干燥,根据实验中为控制温度在140~170℃及选项的沸点进行判断;
(2)由于水蒸气蒸馏可以应用于分离和提纯有机物,所以图2中水蒸气蒸馏后产品在三颈烧瓶中;装置b中长玻璃导管要伸入混合物中,使混合物与水蒸气充分接触,有利于提纯肉桂酸;
(3)温度低肉桂酸钠的溶解度降低,会结晶析出晶体,所以趁热过滤的目的是防止肉桂酸钠结晶而析出堵塞漏斗;
(4)由于盐酸是强酸,所以加入1:1的盐酸的目的是使肉桂酸盐转化为肉桂酸;肉桂酸晶体在水中的溶解度很小,据此答题;
(5)先根据表中密度计算出苯甲醛、乙酸酐的质量,再计算出它们的物质的量,然后理论上生成肉桂酸的质量,最后计算出肉桂酸的产率.
解答 解:(1)乙酸酐易水解,所以仪器必须干燥,
A、由于水的沸点只有100℃,不能通过水浴加热,故A错误;
B、由于甘油而的沸点高于170℃,故B正确;
C、沙子是固体,不便于控制温度,C错误;
D、由于植物油的沸点高于170℃,所以实验中为控制温度在140~170℃需在植物油中加热,故BD,
故答案为:乙酸酐易水解;BD;
(2)水蒸气蒸馏可以应用于分离和提纯有机物,所以图2中水蒸气蒸馏后产品在三颈烧瓶中;装置b中长玻璃导管要伸入混合物中,使混合物与水蒸气充分接触,有利于提纯肉桂酸,
故答案为:产生水蒸气;使混合物与水蒸气充分接触,有利于提纯肉桂酸;三颈烧瓶;
(3)温度低,肉桂酸钠的溶解度降低,会结晶析出晶体,所以趁热过滤的目的是防止肉桂酸钠结晶而析出堵塞漏斗,
故答案为:防止肉桂酸钠结晶而析出堵塞漏斗;
(4)盐酸是强酸,所以加入1:1的盐酸的目的是使肉桂酸盐转化为肉桂酸;肉桂酸晶体在水中的溶解度很小,所以可以用水洗涤,
故答案为:使肉桂酸盐转化为肉桂酸; 水;
(5)5.3g苯甲醛、10.2乙酸酐,二者的物质的量分别是5.3g÷106g/mol=0.05mol、10.2g÷102g/mol=0.1mol,所以根据方程式可知,乙酸酐过量,则理论上生成肉桂酸的质量是0.05mol×148g/mol=7.4g,所以产率是:$\frac{3.1g\\;}{7.4g}$×100%=41.9%,
故答案为:41.9%.
点评 本题主要考查有机物的制备实验,试题综合性强,侧重对学生能力的培养和训练,难度中等,要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论.

| A. | 元素周期表的七个周期永远不会改变 | |
| B. | 元素周期表有九个横行,分为七个周期 | |
| C. | 元素周期表有十八个纵行,分为十六个族 | |
| D. | 元素周期表有十八个纵行,分为十八个族 |
| A. | 温度相同、体积相同的O2和N2 | B. | 质量相等、密度不等的N2和C2H4 | ||
| C. | 体积相同、密度不等的CO和C2H4 | D. | 压强相同、体积相同的O2和H2 |
已知:①过程中生成的中间物质格氏试剂易发生水解反应;
②部分相关物质的沸点如下:
| 物质 | 沸点/℃ |
| 三苯甲醇 | 380 |
| 乙醚 | 34.6 |
| 溴苯 | 156.2 |
请回答下列问题:
(1)装置中玻璃仪器B的名称为冷凝管;装有无水CaCl2的仪器A的作用是防止空气中的水蒸气进入装置,避免格氏试剂水解.
(2)装置中滴加液体未用普通分液漏斗而用滴液漏斗的作用是平衡压强,使漏斗内液体顺利滴下;
(3)制得的三苯甲醇粗产品中含有乙醚、溴苯、氯化铵等杂质,可以设计如图2提纯方案:其中,操作①的名称是蒸馏或分馏;洗涤液最好选用a(填字母序号).
a.水 b.乙醚 c.乙醇 d.苯
检验产品已经洗涤干净的操作为取少量最后一次洗涤液于试管中,滴加硝酸银溶液,若无沉淀生成,则已经洗涤干净,反之则未洗涤干净.
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不反应),充分反应后,测得生成的气体在标准状况下的体积为100.80mL.则产品中三苯甲醇的质量分数为90%.
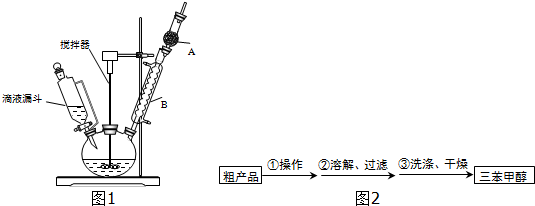

温度、固液比、反应时间、氯离子浓度都对铜的浸出率有较大的影响,下面是实验得出的这几种因素对铜的浸出率影响的变化曲线图(如图2-图5所示)
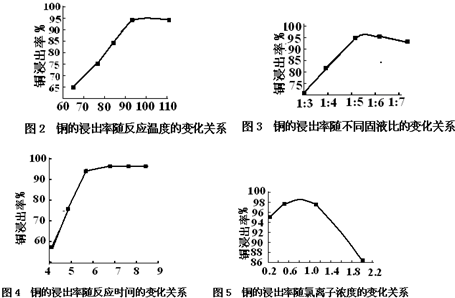
(1)根据实验以及工业生产的实际要求,从图2-图5中得出的最佳工艺条件为(从下表中选出序号)A.
| 反应温度/℃ | 固液比 | c(Cl-)/mol•L-1 | 反应时间/h | |
| A | 95 | 1:5.5 | 0.8 | 6 |
| B | 100 | 1:5.5 | 0.7 | 7 |
| C | 110 | 1:6 | 0.9 | 8 |
(3)副产品FeSO4•7H2O样品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取5.800g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中,
步骤3:用硫酸酸化的0.0100mol/L KMnO4溶液滴定至终点,记录消耗KMnO4溶液体积
步骤4:重复步骤2、步骤3一至两次.
①步骤1中用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管和250mL容量瓶,步骤2量取溶液所用仪器是酸式滴定管.
②写出步骤3反应的离子方程式5Fe2++MnO-4+8H+=5Fe3++Mn2++4H2O:
③数据处理:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 40.01 |
| 2 | 25.00mL | 0.70 | 40.71 |
| 3 | 25.00mL | 0.20 | 39.20 |
④不考虑操作误差,用上述方法测定的样品中FeSO4•7H2O的质量分数偏低(填偏低、偏高或无影响).
| A. | 某山区发现了一种“柴油树”,它产生的树油可替代柴油使用 | |
| B. | 新型材料碳纳米管的化学性质常温下很稳定 | |
| C. | 美国最新研制出一种燃料电池,其能量转化率很高,可能达到100% | |
| D. | 蜘蛛丝(主要成分是蛋白质分子)强度特别大,可以用来制造防弹衣和降落伞绳 |
| A. | Y、Z元素最高价氧化物对应的水化物酸性较强的为H2ZO4 | |
| B. | 离子半径由大到小的顺序为:W>Z>Y | |
| C. | X、Z两种元素的气态氢化物中,X的气态氢化物较稳定,因为X的氢化物分子间有氢键 | |
| D. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.查阅资料:SO2Cl2在常温下为无色液体,极易水解,遇潮湿空气会产生白雾.
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.查阅资料:SO2Cl2在常温下为无色液体,极易水解,遇潮湿空气会产生白雾.