题目内容
【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,如图所示是某厂应用“侯氏制碱法”生产纯碱的工艺流程图,据图回答:
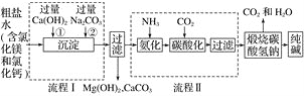
(1)上述流程图中,可循环利用的物质是____________。
(2)流程Ⅰ后过滤所得滤液中含有的溶质有__________。
(3)流程Ⅱ先通入氨气,再通入二氧化碳,如果反过来,二氧化碳的吸收率会降低,这是因为___________。
(4)用一个化学反应方程式表示出流程Ⅱ中发生的总反应____。
(5)工业生产纯碱的流程中,碳酸化时溶液中先析出碳酸氢钠而没有析出氯化铵的原因是_____________________。
【答案】NaCl和二氧化碳 NaOH、氯化钠和碳酸钠 氨气不但溶解度大,而且氨气的水溶液呈碱性,可增大二氧化碳的溶解度,获得更多的碳酸氢铵 NaCl+H2O+NH3+CO2===NaHCO3↓+NH4Cl 相同温度下,碳酸氢钠的溶解度比氯化铵小得多,所以碳酸化过程先析出碳酸氢钠
【解析】
(1)观察流程图分析可循环利用的物质;
(2)根据除杂的过程及反应的方程式分析溶质的成分;
(3)根据氨气溶于水溶液显碱性,有利于二氧化碳的吸收进行解答;
(4)根据反应物和生成物结合流程的反应写出反应的方程式;
(5)根据该温度下碳酸氢钠的溶解度比氯化铵小进行解答。
(1)在流程中能够回收再利用的物质有氯化钠和二氧化碳,故答案为:氯化钠和二氧化碳;
(2)过量的氢氧化钙和氯化镁反应产生氢氧化镁沉淀和氯化钠,过量的碳酸钠和氯化钙反应产生碳酸钙沉淀和氯化钠,和氢氧化钙反应产生碳酸钙沉淀和氯化钠,因此滤液中的溶质有生成的氢氧化钠、生成和原有的氯化钠和过量的碳酸钠,故答案为:氢氧化钠、氯化钠和碳酸钠;
(3)氨气不但溶解度大,而且氨气的水溶液呈碱性,可增大二氧化碳的溶解度,获得更多的碳酸氢铵,所以制氨盐水的过程中要先通入氨气,再通入二氧化碳,故答案为:氨气不但溶解度大,而且氨气的水溶液呈碱性,可增大二氧化碳的溶解度,获得更多的碳酸氢铵;
(4)根据氯化钠、水、氨气和二氧化碳反应生成碳酸氢钠和氯化铵,发生的总反应NaCl+H2O+
NH3+CO2═NaHCO3+NH4Cl,故答案为:NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl;
(5)工业生产纯碱的流程中,碳酸化时溶液中析出碳酸氢钠而没有析出氯化铵的原因是在相同温度下,碳酸氢钠的溶解度比氯化铵小得多,所以碳酸化过程先析出碳酸氢钠,故答案为:相同温度下,碳酸氢钠的溶解度比氯化铵小得多,所以碳酸化过程先析出碳酸氢钠。

 考前必练系列答案
考前必练系列答案【题目】(题文)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

(1)反应Ⅰ:2H2SO4(l)![]() 2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)![]() SO2(g) ΔH3=-297 kJ·mol-1
SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:________________。
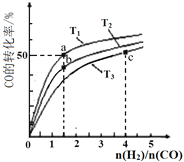
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。

p2_______p 1(填“>”或“<”),得出该结论的理由是________________。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+![]() S↓+2I2+2H2O
S↓+2I2+2H2O
ii.I2+2H2O+_________![]() _________+_______+2 I-
_________+_______+2 I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则a=__________。
②比较A、B、C,可得出的结论是______________________。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________________。