题目内容
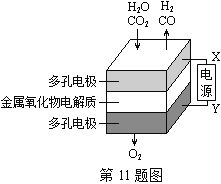
【题目】如图是某反应的能量关系图,下列叙述错误的是( )
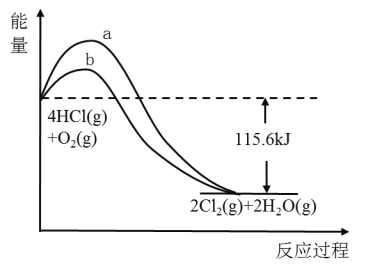
A.反应物总能量高于生成物的总能量
B.曲线b是使用了催化剂的能量变化曲线
C.反应的热化学方程式为:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)+115.6kJ
2Cl2(g)+2H2O(g)+115.6kJ
D.若反应生成2mol液态水,放出的热量低于115.6kJ
【答案】D
【解析】
A.由图看出反应物总能量高,生成物总能量低,反应物总能量高于生成物总能量,故A正确;
B.使用催化剂能降低反应所需活化能,则b为使用催化剂的图象,a为未使用催化剂的图象,故B正确;
C.反应物为:4HCl(g)+O2(g),生成物为:2Cl2(g)+2H2O(g),反应放出热量为115.6kJ,所以热化学方程式为:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)+115.6kJ,故C正确;
2Cl2(g)+2H2O(g)+115.6kJ,故C正确;
D.若生成2mol液态水,液态水比气态水能量低,放热会更多,放出的热量高于115.6kJ,故D错误;
答案选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目