题目内容
20.已知化学式为C12H12的物质其结构简式为 ,该环上的二溴代物有9种同分异构体,由此推断该环上的四溴代物的同分异构体数目有( )
,该环上的二溴代物有9种同分异构体,由此推断该环上的四溴代物的同分异构体数目有( )| A. | 4种 | B. | 9种 | C. | 12种 | D. | 6种 |
分析 利用换元法解答,苯环上的四溴代物可以看作苯环六溴代物其中2个溴原子被2个H原子取代,故二溴代物与四溴代物同分异构体数目相同.
解答 解:苯环上的四溴代物可以看作苯环六溴代物其中2个溴原子被2个H原子取代,故四溴代物与二溴代物同分异构体数目相同,由于二溴代物有9种同分异构体,故四溴代物的同分异构体数目也为9种,故选B.
点评 本题考查同分异构体数目的判断,难度中等,注意利用换元法进行的解答.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
11.下列说法正确的是( )
| A. | 按系统命名法, 的名称为2,7,7-三甲基-3-乙基辛烷 的名称为2,7,7-三甲基-3-乙基辛烷 | |
| B. | 实验证实 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 | |
| C. | DDT的结构简式为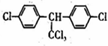 ,分子中最多有14个碳原子共平面 ,分子中最多有14个碳原子共平面 | |
| D. |  的单体是CH3-C≡C-CH3和CH2=CH-CN 的单体是CH3-C≡C-CH3和CH2=CH-CN |
8.在构成原子的各种微粒中,决定元素种类的是( )
| A. | 质子数 | B. | 中子数 | C. | 核外电子数 | D. | 质子数和中子数 |
15.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:(无特殊说明均填元素符号、化学式等化学用语)
(1)在这些元素中,化学性质最不活泼的元素名称是氖,元素原子半径最小的是H,⑧号元素的离子结构示意图为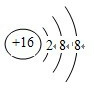 .
.
(2)在上述元素的最高价氧化物对应水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH,既能与强酸反应,又能与强碱反应的化合物的化学式是Al(OH)3.
(3)⑧、⑨号元素的氢化物中还原性较强的是H2S(填化学式).
(4)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O
(5)写出能说明⑨的非金属性比⑧强的一个实验事实氯气与硫化钠反应生成氯化钠和硫单质.
| 主族 周期 | IA | ⅡA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
 .
.(2)在上述元素的最高价氧化物对应水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH,既能与强酸反应,又能与强碱反应的化合物的化学式是Al(OH)3.
(3)⑧、⑨号元素的氢化物中还原性较强的是H2S(填化学式).
(4)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O
(5)写出能说明⑨的非金属性比⑧强的一个实验事实氯气与硫化钠反应生成氯化钠和硫单质.
5.下列属于吸热反应的是( )
| A. | 金属钠与水的反应 | B. | 氢气在氯气中燃烧 | ||
| C. | 浓硫酸的稀释 | D. | Ba(OH)2•8H2O和NH4Cl(固体)混合 |
12.描述或解释下列现象的离子方程式,不正确的是( )
| A. | 碳酸氢铵溶液中加足量石灰水:NH4++HCO3-+Ca2++2OH-=CaCO3↓+NH3•H2O+H2O | |
| B. | 碳酸氢钠溶液与硫酸氢钠溶液反应:HCO3-+H+=CO2↑+H2O | |
| C. | 滴有石蕊的烧碱溶液里通CO2至颜色变红:CO2+2OH-=CO32-+H2O | |
| D. | 漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO |
9.某有机物在O2中充分燃烧,生成等物质的量的H2O水和CO2,则其必须满足的条件是( )
| A. | 分子中的C、H、O的个数比为1:2:3 | B. | 分子中C、H个数比为1:2 | ||
| C. | 该有机物的相对分子质量为14 | D. | 该分子中肯定不含氧元素 |
10.要使有机物 转化为
转化为 ,最佳试剂是( )
,最佳试剂是( )
 转化为
转化为 ,最佳试剂是( )
,最佳试剂是( )| A. | Na | B. | NaHCO3 | C. | Na2CO3 | D. | NaOH |

