��Ŀ����
 ij����С��ͬѧ����ͼװ�ý���ʵ�飬һ��ʱ�����C�缫������ͭ�������Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬һ��ʱ�����C�缫������ͭ�������Իش��������⣮��1��AΪ��Դ��
����
����
������2��E�ĵ缫��ӦʽΪ��
2H++2e-=H2��
2H++2e-=H2��
����3�����ס���װ���е�C��D��E��F�缫��ֻ��һ�ֵ�������ʱ����Ӧ���ʵ����ʵ���֮��Ϊ
2��1��2��2
2��1��2��2
����4���ڳ����£����ñ�װ�ø�����ͭ����H�缫����Ӧ����
ͭ
ͭ
������������������ͭ��3.2gʱ��������Һ��PHֵΪ13
13
��������Һ���Ϊ1L������5���ڵ��һ��ʱ����ڼ��м�������
CuO�������ǵ�ˮ��ʼ���Cu��OH��2Ҳ���ԣ�
CuO�������ǵ�ˮ��ʼ���Cu��OH��2Ҳ���ԣ�
����ʹ��Һ�ָ���ԭ����Ũ�ȣ���������1�����ݵ��ع���ԭ���ж�C�ĵ缫������C�ĵ缫�жϵ�ԴA�ĵ缫��
��2�����ж�E�ĵ缫����ȷ��E�ĵ缫��Ӧʽ��
��3�����ж����ɵĵ��ʣ��ٸ��ݵ�ʧ����������ж������ʵ���֮�ȣ�
��4�����ݵ��ԭ���ж�H�缫���ϣ�����ͭ�������ӵĹ�ϵʽ�������Һ��PH��
��5�����ݵ���������жϣ�
��2�����ж�E�ĵ缫����ȷ��E�ĵ缫��Ӧʽ��
��3�����ж����ɵĵ��ʣ��ٸ��ݵ�ʧ����������ж������ʵ���֮�ȣ�
��4�����ݵ��ԭ���ж�H�缫���ϣ�����ͭ�������ӵĹ�ϵʽ�������Һ��PH��
��5�����ݵ���������жϣ�
����⣺��1��C�缫����ͭ������C�缫�Ϸ�����ԭ��Ӧ������C�缫�������������������Ǹ���������AΪ�������ʴ�Ϊ��������
��2��C����������D��������E��������F���������������������Ϸ�����ԭ��Ӧ����Һ�������ӵķŵ��������������ӣ����������ӷŵ磬�ʴ�Ϊ��2H++2e-=H2��
��3���������ӵķŵ�˳���жϣ��ס���װ����C��D��E��F�ĸ��缫�Ϸֱ����ɵ�������Cu��O2��H2��
Cl2�����ݵ�ʧ��������ȣ����������ʼ�Ĺ�ϵʽΪ 2Cu--O2--2 H2--2Cl2���������ʵ���֮�ȵ��ڼ�����֮��֪�����ʵ���֮��Ϊ2��1��2��2���ʴ�Ϊ��2��1��2��2��
��4����������֪��GΪ������HΪ���������ݵ��ԭ�����Ʋ����������Ƽ�������������H�缫����Ӧ����ͭ��
��װ���е�������Դ��ˮ��һ��ˮ���ӵ����һ�������Ӻ�һ�����������ӣ���������������һ������ӣ���������Ӻ����������ӵĹ�ϵʽΪ H2 --2 OH -�����ݵ�ʧ��������ȣ���װ����������ͭ����װ���������Ĺ�ϵʽΪ
Cu--H2���������������Ӻ�ͭ�Ĺ�ϵʽΪ
Cu--2 OH -
64g 2mol
3.2g 0.1mol
����C��OH-��=0.1 mol/L����C��H+��=1��10-13 mol/L������PH=13���ʴ�Ϊ��ͭ��13��
��5����װ���е�ⷴӦ����ʽΪ 2CuSO4+2H2O
2Cu+O2��+2H2SO4
�ɷ���ʽ֪��������������ͭ�����������Լ�������ͭ���ɣ��ʴ�Ϊ��CuO�������ǵ�ˮ��ʼ���Cu��OH��2Ҳ���ԣ�
��2��C����������D��������E��������F���������������������Ϸ�����ԭ��Ӧ����Һ�������ӵķŵ��������������ӣ����������ӷŵ磬�ʴ�Ϊ��2H++2e-=H2��
��3���������ӵķŵ�˳���жϣ��ס���װ����C��D��E��F�ĸ��缫�Ϸֱ����ɵ�������Cu��O2��H2��
Cl2�����ݵ�ʧ��������ȣ����������ʼ�Ĺ�ϵʽΪ 2Cu--O2--2 H2--2Cl2���������ʵ���֮�ȵ��ڼ�����֮��֪�����ʵ���֮��Ϊ2��1��2��2���ʴ�Ϊ��2��1��2��2��
��4����������֪��GΪ������HΪ���������ݵ��ԭ�����Ʋ����������Ƽ�������������H�缫����Ӧ����ͭ��
��װ���е�������Դ��ˮ��һ��ˮ���ӵ����һ�������Ӻ�һ�����������ӣ���������������һ������ӣ���������Ӻ����������ӵĹ�ϵʽΪ H2 --2 OH -�����ݵ�ʧ��������ȣ���װ����������ͭ����װ���������Ĺ�ϵʽΪ
Cu--H2���������������Ӻ�ͭ�Ĺ�ϵʽΪ
Cu--2 OH -
64g 2mol
3.2g 0.1mol
����C��OH-��=0.1 mol/L����C��H+��=1��10-13 mol/L������PH=13���ʴ�Ϊ��ͭ��13��
��5����װ���е�ⷴӦ����ʽΪ 2CuSO4+2H2O
| ||
�ɷ���ʽ֪��������������ͭ�����������Լ�������ͭ���ɣ��ʴ�Ϊ��CuO�������ǵ�ˮ��ʼ���Cu��OH��2Ҳ���ԣ�
�������������й����ļ�����жϣ��������й����ļ�����ж���Ҫ�������¼����棺����ֱ����Դ�ṩ�ĵ���������������Һ��PH����ѧʽ�ȣ����������ǵ�ʧ�����غ㣬�����½��ⷽ����
1�����ݵ����غ㷨���㣻
2�������ܷ�Ӧʽ���㣻
3�����ݹ�ϵʽ���㣻
1�����ݵ����غ㷨���㣻
2�������ܷ�Ӧʽ���㣻
3�����ݹ�ϵʽ���㣻

��ϰ��ϵ�д�
�����Ŀ
 ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮ ��2008?��ݸģ�⣩ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
��2008?��ݸģ�⣩ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮ ����������������������أ�
����������������������أ� ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣺
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣺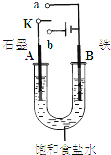 ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮