题目内容
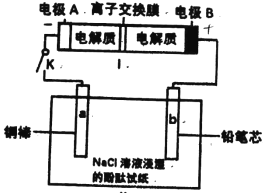
【题目】下图是一种正投入生产的大型蓄电系统,放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是( )
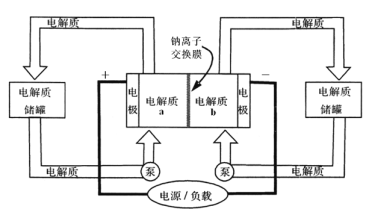
A. 放电时,负极反应为3NaBr-2e-=NaBr3+2Na+
B. 充电时,阳极反应为2Na2S2-2e-=Na2S4+2Na+
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 用该电池电解饱和食盐水,产生2.24 L H2时,b池生成17.40gNa2S4
【答案】C
【解析】
由题意可知,放电时,负极上Na2S2被氧化为Na2S4,正极上NaBr3被还原为NaBr,则左储罐电解质为NaBr3/NaBr,右储罐电解质为Na2S2/Na2S4。
A、放电时,负极上Na2S2被氧化为Na2S4,电极反应式为:2Na2S2-2e- =Na2S4+2Na+,故A错误;
B、充电时,电池的正极与电源正极相连,作阳极,阳极上NaBr被氧化为NaBr3,电极反应式为:3NaBr-2e-=NaBr3+2Na+,故B错误;
C、放电时,阳离子向正极移动,则离子Na+经过离子交换膜,由b池移向a池,故C正确;
D、没有确定是否为标准状况,无法计算氢气的物质的量,则无法计算b池生成Na2S4质量,故D错误;
答案选C。

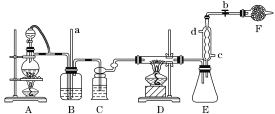
【题目】一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。某化学兴趣小组设计如图装置以制备Cl2O(支撑及夹持装置已省略)。
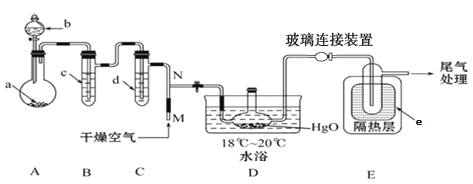
已知:① a中固体试剂是MnO2,b中试剂是浓盐酸。 ②Cl2O的部分性质如下表。
熔点 | 沸点 | 制备方法 |
-120.6 ℃ | 3.8℃ | 2HgO+2Cl2 = Cl2O+HgCl2·HgO |
请回答:
(1)指出该制备装置中存在的一个明显错误______________(经改进后进行有关实验)。
(2)装置C中盛有的试剂是______________。
(3)写出装置A中制备Cl2的化学方程式__________。
(4)装置D中采用18℃~20℃水浴的原因之一是如温度过低,反应速率慢,另一个可能的原因是 ___________。
(5)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,装置D、E间采用这种连接方式的理由是____________。
(6)Cl2O是市场上一种比较理想的饮水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2消毒能力是等质量Cl2O的_________倍(结果保留两位小数)
(7)文献报道说,Cl2O的另一种制备方法是利用Cl2与足量的Na2CO3溶液反应来制得,写出该反应的化学方程式:_________。