题目内容
5.已知HA的酸性比HB的酸性强.现有物质的量浓度和体积均相同的NaA和NaB两种溶液,已知前者溶液中离子数目为n1,后者溶液中离子数目为n2.下列关系正确是( )| A. | n1=n2 | B. | n1>n2 | C. | n1<n2 | D. | c(A-)<c(B-) |
分析 HA的酸性比HB的酸性强,HA的电离程度大于HB,则其酸根离子水解程度A-<B-,相同温度下,物质的量浓度和体积均相同的NaA和NaB两种溶液中两种盐的物质的量相等,溶液中存在电荷守恒和物料守恒,根据电荷守恒判断.
解答 解:HA的酸性比HB的酸性强,HA的电离程度大于HB,则其酸根离子水解程度A-<B-,相同温度下,物质的量浓度和体积均相同的NaA和NaB两种溶液中两种盐的物质的量相等,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(A-)、c(Na+)+c(H+)=c(OH-)+c(B-),两种溶液中离子浓度分别是其溶液中所有阳离子浓度的2倍,
因为酸根离子水解程度A-<B-,所以NaA溶液中氢离子浓度大于NaB,两种溶液中钠离子浓度相等,所以NaA溶液中离子个数大于NaB离子个数,即n1>n2,
故选B.
点评 本题以离子个数比较为载体考查了盐类水解,明确电离平衡常数与酸根离子水解程度的关系是解本题关键,然后再采用电荷守恒、离子代换等方法来分析解答,难度中等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
15. 二氧化碳是造成温室效应的主要气体,二氧化碳的回收再利用是减缓温室效应的有效途径之一.
二氧化碳是造成温室效应的主要气体,二氧化碳的回收再利用是减缓温室效应的有效途径之一.
(1)二氧化碳重整可用于制取甲烷,已知:
CH4(g)+CO2(g)?2CO(g)+2H2(g)△H1=+247kJ•mol-1
CH4(g)+H2O(g)?CO(g)+3H2(g)△H2=+205kJ•mol-1
则反应CO2(g)+4H2(g)?CH4(g)+2H2O(g)的△H3=-163kJ/mol.
(2)一定压强下,在某恒容密闭容器中,充入H2和CO2发生反应:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),其起始投料比、温度与CO2的转化率的关系如图所示.
①降低温度,平衡向逆反应 方向移动.
②在700K,起始投料比$\frac{n({H}_{2})}{n(C{O}_{2})}$=1.5时,H2 的转化率为40%.
(3)CO2和H2在一定条件下可合成二甲醚:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H.在一定压强下,将2.5molH2与a molCO2置于容积为1L的密闭容器中,发生上述反应,达到平衡状态时,测得反应的实验数据如下表:
①x、y的大小关系为B.
A.x=y B.x>y C.x<y D.无法判断
②下列关于该反应叙述正确的是ABC
A.该反应的△H<0,△S<0
B.该反应的平衡常数随温度升高而减小
C.转化率分别为z、w时,达到平衡的时间前者长
D.转化率分别为y、w时,平衡常数不同.
 二氧化碳是造成温室效应的主要气体,二氧化碳的回收再利用是减缓温室效应的有效途径之一.
二氧化碳是造成温室效应的主要气体,二氧化碳的回收再利用是减缓温室效应的有效途径之一.(1)二氧化碳重整可用于制取甲烷,已知:
CH4(g)+CO2(g)?2CO(g)+2H2(g)△H1=+247kJ•mol-1
CH4(g)+H2O(g)?CO(g)+3H2(g)△H2=+205kJ•mol-1
则反应CO2(g)+4H2(g)?CH4(g)+2H2O(g)的△H3=-163kJ/mol.
(2)一定压强下,在某恒容密闭容器中,充入H2和CO2发生反应:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),其起始投料比、温度与CO2的转化率的关系如图所示.
①降低温度,平衡向逆反应 方向移动.
②在700K,起始投料比$\frac{n({H}_{2})}{n(C{O}_{2})}$=1.5时,H2 的转化率为40%.
(3)CO2和H2在一定条件下可合成二甲醚:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H.在一定压强下,将2.5molH2与a molCO2置于容积为1L的密闭容器中,发生上述反应,达到平衡状态时,测得反应的实验数据如下表:
| 温度/K CO2转化率/% a/mol | 500 | 600 | 700 | 800 |
| 1.67 | x | 33 | ||
| 1.25 | 60 | 43 | y | |
| 0.83 | z | 32 | w |
A.x=y B.x>y C.x<y D.无法判断
②下列关于该反应叙述正确的是ABC
A.该反应的△H<0,△S<0
B.该反应的平衡常数随温度升高而减小
C.转化率分别为z、w时,达到平衡的时间前者长
D.转化率分别为y、w时,平衡常数不同.
20.某实验小组设计实验测定Na2S04和Na2C03混合物中各组分的含量.
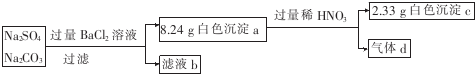
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 沉淀a的主要成分是BaS04和BaC03 | |
| B. | 滤液b中Na+的物质的量为0.08 mol | |
| C. | 气体d在标准状况下的体积为224 mL | |
| D. | 原混合物中Na2S04与Na2C03的物质的量之比为1:3 |
10.下列说法正确的是( )
| A. | 由H原子形成1 mol H-H键要吸收热量 | |
| B. | 所有燃烧反应都是放热反应 | |
| C. | 在稀溶液中,1 mol酸与1 mol碱发生中和反应生成水时所释放的热量称为中和热 | |
| D. | 在一定条件下,1mol H2 与足量的Cl2、Br2、I2 分别反应,放出热量关系是I2>Br2>Cl2 |
17.某小组用如图装置进行实验,下列说法正确的是( )


| A. | 盐桥中的电解质可以用KC1 | |
| B. | 导线中流过0.2mol电子时,加入4.9gCu(OH)2,CuSO4溶液可恢复原组成 | |
| C. | 闭合K,石墨电极上只生成铜 | |
| D. | 闭合K,外电路电流方向为Fe电极→石墨电极 |
15.下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A. | 10mL0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合c(Clˉ)>c(Na+)>c(OHˉ)>c(H+) | |
| B. | 10mL0.1mol/LNH4 Cl溶液与5mL0.2mol/LNaOH溶液混合c(Na+)=c(Clˉ)>c(OHˉ)>c(H+) | |
| C. | 10mL0.1mol/LCH3COOH溶液与5mL0.2mol/LNaOH溶液混合c(Na+)=c(CH3COOˉ)>c(OHˉ)>c(H+) | |
| D. | 10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合 c(Clˉ)>c(NH4+)>c(OHˉ)>c(H+) |
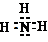 .
.


