题目内容
1.合成纤维是以空气、煤、石油等作为起始原料经化学合成而生产出来的纤维.主要包括六大纶,其中保暖性最好的是有人造羊毛之称的腈纶.涤纶是聚对苯二甲酸乙二酯,制备原理为: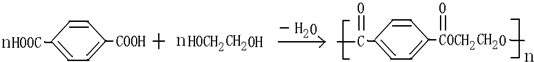
该反应属于缩聚反应(填“加聚反应”或“缩聚反应”),其单体为对苯二甲酸和乙二醇.
分析 合成纤维是以空气、煤、石油等作为起始原料经化学合成而生产出来的纤维.保暖性最好的是有人造羊毛之称的腈纶.链节中含有酯基结构的高聚物,按酯基中碳氧单键断裂,羰基上加羟基,氧原子上加氢原子即得高聚物单体.
解答 解:合成纤维是以空气、煤、石油等作为起始原料经化学合成而生产出来的纤维.保暖性最好的是有人造羊毛之称的腈纶.链节中含有酯基,聚酯纤维是由乙二醇(HO-CH2-CH2-OH)和对苯二甲酸(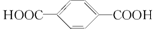 )通过缩聚形成的,故答案为:煤;石油;腈纶;缩聚反应;对苯二甲酸和乙二醇.
)通过缩聚形成的,故答案为:煤;石油;腈纶;缩聚反应;对苯二甲酸和乙二醇.
点评 本题以高聚物的结构为载体,考查酯化反应、聚合反应等,难度中等,关键清楚酯化反应的机理判断单体.

练习册系列答案
相关题目
11.下列离子方程式正确的是( )
| A. | 氯化镁溶液中滴入NaOH溶液:MgCl2+2OH-═Mg(OH)2↓+2Cl- | |
| B. | 碳酸氢钠溶液与氢氧化钠反应:OH-+HCO3-═CO2+H2O | |
| C. | 铁粉加入稀盐酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氨气通入硝酸中:NH3+H+═NH4+ |
12.某气态烷烃与丙炔的混合气体22.4L ( 标准状况 ),完全燃烧后生成121g CO2和40.5g H2O,则原混合气体中烷烃的分子式为( )
| A. | C3H8 | B. | CH4 | C. | C2H6 | D. | C4H10 |
16.下列说法正确的是( )
| A. | 福尔马林是一种良好的杀菌剂,但不可用来消毒饮用水 | |
| B. | 由于人体不能消化纤维素,所以人吃纤维素没用 | |
| C. | 抗生素有很好的抗菌作用,得到广泛的应用,属于非处方药 | |
| D. | 肠溶片咀嚼后更有利于在肠道的吸收 |
13.下列有关物质的性质及其解释都正确的是( )
| A. | 在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,在反应中体现硫酸的还原性 | |
| B. | 向一定体积的稀硫酸中加入一定量的Cu、Fe和Fe2O3混合物,反应后有固体剩余,其可能只含铁 | |
| C. | 氢氧化镁和氢氧化铝是常见的阻燃剂,它们分解时发生吸热反应 | |
| D. | 铝在空气中表现为良好的抗腐蚀性,说明铝极难与氧气反应 |
10.下列化学用语的相关表述正确的是( )
| A. | H+(aq)+OH-(aq)=H2O(l)△H=-a kJ/mol,故1 mol NaOH固体与足量的稀盐酸反应,放出热量为akJ | |
| B. | 因CuSO4•5H2O(s)═CuSO4(s)+5H2O(1)△H=+b kJ/mol,故1 mol CuSO4(s)溶于足量水时,放出热量为bkJ | |
| C. | 因氢气的燃烧热为c kJ/mol,故电解水的热化学方程式为:2H2O(1)═2H2(g)+O2(g)△H=+c kJ/mol | |
| D. | 因N2(g)+3H2(g)?2NH3(g)△H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于dkJ |
11.如表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | A2+与D2-的核外电子数相等 | |
| B. | B与E形成的化合物具有两性 | |
| C. | 氢化物的稳定性为H2E<H2D | |
| D. | C单质与浓度相等的稀盐酸反应比A快 |