题目内容
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
| A.X、Y、Z、W的原子半径依次减小 |
| B.W与X形成的化合物中只含离子键 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
A
解析

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
下列说法中,正确的是 ( )
A.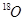 原子核内的中子数为8 原子核内的中子数为8 |
B.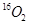 和 和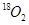 的化学性质几乎相同 的化学性质几乎相同 |
C.H2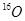 与H2 与H2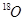 质子数不同 质子数不同 |
| D.H2和D2属于同位素 |
短周期元素X原子核外的电子处于n个电子层上,最外层电子数为(2n+1),核内质子数为(2n2-1)。有关X的说法中不正确的是
| A.X元素气态氢化物的水溶液不可能呈酸性 |
| B.X能形成化学式为NaXO3的含氧酸钠盐 |
| C.X原子的最外层电子数和核电荷数不可能为偶数 |
| D.X元素常见单质的化学式为X2 |
下列说法正确的是 ( )。
| A.原子核都是由质子和中子构成的 |
| B.同位素的化学性质基本相同,其物理性质不一定相同 |
| C.第ⅠA族元素铯的两种同位素,137Cs比133Cs多4个质子 |
| D.质子数相同的微粒都属于同种元素 |
元素的原子结构决定其性质和周期表中的位置。下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 |
| D.元素周期表中位于金属和非金属的分界线附近的元素属于过渡元素 |
化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=(NH?3通过如下反应制得:3CH4+2?HB=NH)3+6H2O=3CO2+6H3BNH3。对合成A反应方程式的讨论中不正确的是( )
| A.反应前后碳原子的杂化类型不变 |
| B.键角的大小关系:CO2>CH4>H2O |
| C.第一电离能大小关系:N>O>C>B>H |
| D.生成物H3BNH3中存在配位键 |
某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是 ( )。
| A.电子排布式为1s22s22p63s23p63d34s2 |
| B.该元素为V |
| C.该元素为ⅡA族元素 |
| D.该元素位于d区 |
短周期元素X、Y、Z、W的原子序数依次增大,X是形成化合物最多的元素且X常见化合价为+1和-1,Y原子最外层电子数是次外层的3倍;Z与X处于同一主族,W的原子序数是Y的2倍。下列叙述不正确的是( )
| A.原子半径的大小顺序:rZ>rW>rY>rX |
| B.元素Y的简单气态氢化物的热稳定性比W的弱 |
| C.化合物Z2Y2与X2Y反应时,Z2Y2既是氧化剂又是还原剂 |
| D.由X、Y、Z、W四种元素组成的化合物其水溶液一定显酸性 |
V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
| | Y | V | | |
| X | | | | W |
Z为第四周期常见元素,该元素是人体血液中血红蛋白最重要的组成金属元素。V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成。下列说法正确的是( )。
A.原子半径:X>Y>V>W
B.X、W的质子数之和与最外层电子数之和的比值为2∶1
C.甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键
D.少量Z的单质与过量W的单质可化合生成ZW2