题目内容
元素的原子结构决定其性质和周期表中的位置。下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 |
| D.元素周期表中位于金属和非金属的分界线附近的元素属于过渡元素 |
C
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
据报道,2012年俄罗斯科学家再次合成117号元素。本次实验生成了6个新原子,其中5个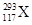 ,1个
,1个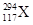 。下列关于
。下列关于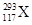 和
和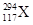 的说法不正确的是( )
的说法不正确的是( )
| A.是两种核素 | B.互为同位素 | C.中子数分别为176和177 | D.电子数相差1 |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的内层电子总数是最外层电子数的5倍。下列说法中不正确的是( )
| A.W、M的某种单质可作为水处理中的消毒剂 |
| B.电解YW2的熔融物可制得Y和W的单质 |
| C.相同条件下,W的氢化物水溶液酸性比Z弱 |
| D.X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
| A.NH4Cl=NH3↑+HCl↑ |
| B.NH3+CO2+H2O=NH4HCO3 |
| C.2NaOH+Cl2=NaCl+NaClO+H2O |
| D.2Na2O2+2CO2=2Na2CO3+O2 |
已知X为第三周期元素的原子,该原子要达到8电子稳定结构,则需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是( )
| A.X元素最高价氧化物对应的水化物一定是强酸 |
| B.X元素的氢化物的化学式一定为H2X |
| C.X的单质一定是良好的半导体材料 |
| D.X元素的氧化物一定能与烧碱反应 |
下列说法中错误的是( )。
| A.SO2、SO3都是极性分子 |
| B.在NH4+和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越弱 |
| D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
| A.X、Y、Z、W的原子半径依次减小 |
| B.W与X形成的化合物中只含离子键 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
 ,下列原子中,与氟元素原子的化学性质相似的是( )
,下列原子中,与氟元素原子的化学性质相似的是( ) 