题目内容
下列说法不正确的是
| A.SO2中S原子含1对孤电子对 | B.BeCl2是直线形分子 |
| C.SO3的空间构型为平面三角形 | D.H20的VSEPR构型和空间构型都是V形 |
D
A、正确,各用一个电子分别与两个氧原子形成δ键,用两个电子和氧原子的各一个电子,形成一个三中心四电子的大π键,还有两个电子形成1对孤电子对;B、正确,Be原子sp杂化;C正确,S原子SP2杂化。D、不正确,H20的VSEPR构型是四面体,空间构型是V形;选D。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
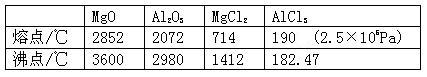
 (2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。 .0g。通过计算请回答下列问题(请写出计算过程)。
.0g。通过计算请回答下列问题(请写出计算过程)。 的气体体积;
的气体体积; 2)开始析出MgSO4·xH2O晶体时溶液的质量分数;
2)开始析出MgSO4·xH2O晶体时溶液的质量分数; 2个O2-相紧邻
2个O2-相紧邻