题目内容
将一定量的锌与100mL18.5mol/L浓硫酸充分反应,锌完全溶解,同时生成16.8L气体 (标准状况),将反应后的溶液稀释到1L,测得溶液的c(H+)=1mol/L,则下列叙述中错误的是
| A.气体A为二氧化硫和氢气的混合物 |
| B.气体A中二氧化硫和氢气的体积比为4:1 |
| C.反应中共消耗锌95.5g |
| D.反应中共转移电子1.5mol |
C
解析试题分析:由题意知原溶液n(H2SO4)=1.85mol,产生n(气体)=16.8L/22.4L/mol=0.75mol,剩余n(H+)=1mol。无论气体A是否为二氧化硫和氢气的混合物,都是得到2个电子的产物,所以反应中共转移0.75mol×2=1.5mol,D正确;根据得失电子守恒,反应过程中只有Zn失电子,所以Zn的物质的量为0.75mol,其质量为48.75g,C错误;反应后的溶液为ZnSO4和H2SO4的混合液,根据元素守恒,得被还原的SO42-为1.85-0.75-0.5=0.6mol,即产生二氧化硫的物质的量为0.6mol,则气体中必有氢气,其物质的量为0.75mol-0.6mol=0.15mol,它们的体积比也为物质的量比为4:1,AB正确,答案选C。
考点:考查锌与浓硫酸反应气体产物的分析计算,元素守恒、得失电子守恒规律的应用

将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解(产生气体全部逸出),冷却后将溶液稀释至1000ml,测得c(H+)=0.84mol/L;若要使稀释后溶液中的Cu2+沉淀完全,应加入6.0mol/L的NaOH溶液的体积为:
| A.100mL | B.160mL | C.240mL | D.307mL |
去年下半年我省雾霾天气十分严重。PM2.5细颗粒物含有的毒性物质来源之一是汽车尾气排放。通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx+CO—催化剂→N2+CO2,下列关于此反应的说法中,不正确的是
| A.所涉及元素的第一电离能:N>O>C |
| B.当x=2时,每生成1molN2,转移电子数为4mol |
C.等物质的量N2和CO2中,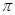 键的个数比为1:1 键的个数比为1:1 |
| D.氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
将a g铝粉加入过量NaOH溶液中充分反应后,铝粉完全溶解,并收集到标准状况下b L氢气,所得溶液中共有c个AlO2-,反应中转移电子d个。则阿伏加德罗常数(NA)可表示为( )
A.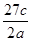 | B.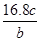 | C.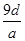 | D.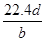 |
根据以下实验事实,判断选项中四种微粒在酸性条件下,氧化性由强到弱的顺序是( )
(1)向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫红色;
(2)向FeCl2溶液中加入氯水,再加入KSCN溶液,溶液呈红色;
(3)向KMnO4溶液中加入浓盐酸,振荡后紫色褪去。
| A.I2>Cl2>Fe3+>MnO4- |
| B.MnO4->Cl2>Fe3+>I2 |
| C.Cl2>I2>Fe3+,MnO4->Fe3+ |
| D.Fe3+>MnO4->Cl2>I2 |
已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中的Cl-、Br-、I-的物质的量之比改变成4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的 ( )。
A.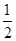 | B.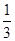 | C.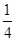 | D.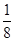 |
美国宇航局“凤凰”号火星登陆器的显微、电子化学及传导分析仪对两份土壤样本的分析发现,火星北极区表层土壤可能含有高氯酸盐,可创造不利于任何潜在生命的恶劣环境。则下列说法错误的是 ( )
| A.含有高氯酸盐的土壤不利于生命存在与高氯酸盐具有较强的氧化性有关 |
| B.当元素处于最高价态时一定具有强氧化性 |
| C.可以考虑用加入亚铁盐等还原性物质的方法改善这种土壤 |
| D.一定条件下高氯酸盐能与浓盐酸反应生成氯气 |
物质的量之比为1∶3的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,下列说法正确的是 ( )。
| A.在此反应中硝酸体现强氧化性,全部被还原 |
| B.向反应后的溶液中再加入金属铁,不再发生化学反应 |
| C.该反应中被还原的硝酸与未被还原的硝酸之比为1∶4 |
| D.该反应中被还原的硝酸与未被还原的硝酸之比为1∶5 |
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
其中第①步中存在平衡:2CrO42- (黄色)+2H+??Cr2O72- (橙色)+H2O。下列有关说法正确的是( )
| A.第①步当2v(Cr2O72-)=v(CrO42-)时,达到了平衡状态 |
| B.对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42-的生成 |
| C.第②步中,还原0.1 mol Cr2O72-需要45.6 g FeSO4 |
| D.第③步沉淀剂a可以使用NaOH等碱性物质 |