题目内容
3.肉桂醛是一种食用香精,它广泛用于牙膏、洗涤剂、糖果以及调味品中.工业上可通过下列反应制备: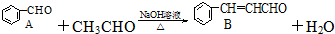
(1)请推测B侧链上可能发生反应的类型:加成反应、氧化反应.(任填两种)
(2)请写出两分子乙醛在上述条件下反应的化学方程式:2CH3CHO$→_{△}^{稀NaOH溶液}$CH3CH=CHCHO+H2O.
(3)请写出A与新制氢氧化铜反应的方程式:
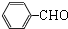 +2Cu(OH)2$\stackrel{△}{→}$c
+2Cu(OH)2$\stackrel{△}{→}$c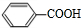 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.(4)请写出同时满足括号内条件下B的所有同分异构体的结构简式:
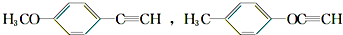
(①分子中不含羰基和羟基;②是苯的对二取代物;③除苯环外,不含其他环状结构.)
分析 (1)侧链含有碳碳双键、醛基,可以发出加成反应、氧化反应、加聚反应等;
(2)由信息可知,两分子乙醛反应生成CH3CH=CHCHO与水;
(3)苯甲醛与新制氢氧化铜反应生成苯甲酸、氧化亚铜与水;
(4)B的同分异构体符合:是苯的对二取代物,除苯环外,不含其他环状结构,分子中不含羰基和羟基,两个侧链为-OCH3、-C≡CH或-CH3、-OC≡CH.
解答 解:(1)B分子侧链上含有碳碳双键和醛基官能团,含碳碳双键可以发生加成反应、加聚和氧化反应,含醛基,可发生氧化、加成、还原反应等,
故答案为:加成反应、氧化反应;
(2)由题目中反应可知,两分子乙醛反应的化学方程式为:2CH3CHO$→_{△}^{稀NaOH溶液}$CH3CH=CHCHO+H2O,
故答案为:2CH3CHO$→_{△}^{稀NaOH溶液}$CH3CH=CHCHO+H2O;
(3)苯甲醛与新制氢氧化铜反应生成苯甲酸、氧化亚铜与水,反应方程式为: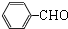 +2Cu(OH)2$\stackrel{△}{→}$c
+2Cu(OH)2$\stackrel{△}{→}$c +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
故答案为: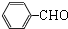 +2Cu(OH)2$\stackrel{△}{→}$c
+2Cu(OH)2$\stackrel{△}{→}$c +Cu2O↓+2H2O;
+Cu2O↓+2H2O;
(3)B的同分异构体符合:是苯的对二取代物,除苯环外,不含其他环状结构,分子中不含羰基和羟基,两个侧链为-OCH3、-C≡CH或-CH3、-OC≡CH.符合条件的同分异构体的结构简式为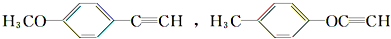 ,
,
故答案为: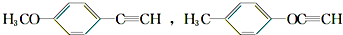 .
.
点评 本题考查有机物的结构与性质,注意把握官能团与性质的关系,侧重醛的性质及同分异构体的考查,题目难度不大.

练习册系列答案
相关题目
12.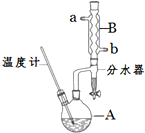 正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:
正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:
2CH3CH2CH2CH2OH$?_{135℃}^{浓硫酸}$(CH3CH2CH2CH2)2O+H2O
反应物和产物的相关数据如下
合成反应:
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间.
分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70mL水的分液漏斗中,振荡后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为先加入正丁醇,再加入浓硫酸.
(2)加热A前,需先从b(填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去浓硫酸,振荡后静置,粗产物应从分液漏斗的上(填“上”或“下”)口分离出.
(4)步骤④中最后一次水洗的目的为洗去有机层中残留的NaOH及中和反应生成的盐.
(5)步骤⑤中,加热蒸馏时应收集d(填选项字母)左右的馏分.
a.100℃b. 117℃c. 135℃d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为正丁醇,下层液体的主要成分为水.
(7)本实验中,正丁醚的产率为34%.(保留两位有效数字)
 正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:
正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH$?_{135℃}^{浓硫酸}$(CH3CH2CH2CH2)2O+H2O
反应物和产物的相关数据如下
| 相对分子质量 | 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间.
分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70mL水的分液漏斗中,振荡后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为先加入正丁醇,再加入浓硫酸.
(2)加热A前,需先从b(填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去浓硫酸,振荡后静置,粗产物应从分液漏斗的上(填“上”或“下”)口分离出.
(4)步骤④中最后一次水洗的目的为洗去有机层中残留的NaOH及中和反应生成的盐.
(5)步骤⑤中,加热蒸馏时应收集d(填选项字母)左右的馏分.
a.100℃b. 117℃c. 135℃d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为正丁醇,下层液体的主要成分为水.
(7)本实验中,正丁醚的产率为34%.(保留两位有效数字)
14.在体积一定的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)?CO(g)+H2O(g)其化学平衡常数K和温度t的关系如表,回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$.
(2)该反应为吸热反应(选填吸热、放热).
(3)能判断该反应是否达到化学平衡状态的依据是bc(多选不得分).
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)某温度下SO2的转化反应的2SO2(g)+O2(g)?2SO3(g)平衡常数K=532.4.
下面三个混合体系中各物质的浓度如下表:
试判断各体系反应进行的方向:体系(2)正向;体系(2):已平衡(填正向、逆向或已平衡).
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$.
(2)该反应为吸热反应(选填吸热、放热).
(3)能判断该反应是否达到化学平衡状态的依据是bc(多选不得分).
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)某温度下SO2的转化反应的2SO2(g)+O2(g)?2SO3(g)平衡常数K=532.4.
下面三个混合体系中各物质的浓度如下表:
| 体系 | c(SO2) mol/L | c(O2) mol/L | c(SO3) mol/L | 浓度商 |
| (1) | 0.0600 | 0.400 | 2.000 | 不填 |
| (2) | 0.0960 | 0.300 | 0.500 | 不填 |
| (3) | 0.0862 | 0.263 | 1.020 | 不填 |
11.下列叙述正确的是( )
| A. | 除0族元素外,短周期元素的最高化合价在数值上都等于该元素所属族的族序数 | |
| B. | 在周期表里,主族元素所在的族序数等于原子核外电子数 | |
| C. | 副族元素没有非金属元素 | |
| D. | 元素的原子序数越大,其原子半径也越大 |
18.等物质的量的下列烃,分别完全燃烧,消耗氧气最少的是( )
| A. | 甲烷 | B. | 甲苯 | C. | 乙炔 | D. | 乙烷 |
8.下列离子方程式书写正确的是( )
| A. | 过氧化钠与水的反应:O2-+H2O=2OH- | |
| B. | 金属钠与水的反应:Na+H2O=Na++OH-+H2↑ | |
| C. | 金属钠与硫酸铜溶液的反应:2Na+Cu2+=Cu+2Na+ | |
| D. | 硫酸氢钠溶液与碳酸氢钠溶液的反应:H++HCO3-=H2O+CO2↑ |
15.下列离子方程式书写正确的是( )
| A. | 稀 H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 氯气和水反应:Cl2+H2O═Cl-+ClO-+2H+ | |
| C. | 碳酸钡与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 氯气和石灰乳反应:Ca(OH)2+Cl2═Ca2++Cl-+ClO-+H2O |
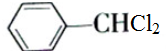 ,沸点206℃)是合成苯甲醛的中间体,实验室合成苄叉二氯的装置如图所示.
,沸点206℃)是合成苯甲醛的中间体,实验室合成苄叉二氯的装置如图所示.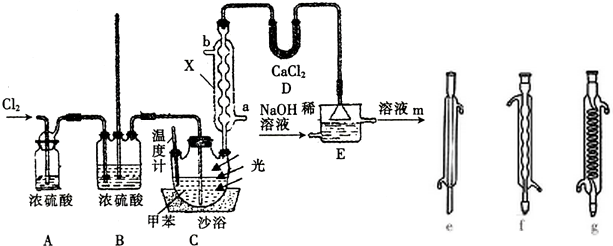
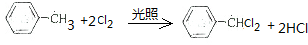 .
.