题目内容
15.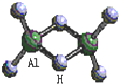 科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上.最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关推测肯定不正确的是( )
科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上.最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关推测肯定不正确的是( )| A. | Al2H6跟水的反应可能是氧化还原反应,产物之一可能是氢氧化铝 | |
| B. | Al2H6在空气中完全燃烧,产物为氧化铝和水 | |
| C. | Al2H6分子是极性分子 | |
| D. | 氢铝化合物可能成为未来的储氢材料和火箭燃料 |
分析 A.Al2H6与水反应生成氢氧化铝和氢气,该反应中H元素化合价由-1价、+1价变为0价;
B.Al2H6在空气中燃烧生成Al的氧化物和H的氧化物;
C.正负电荷重心重合的分子是非极性分子,不重合的分子是极性分子;
D.氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高,能和水反应生成氢氧化铝和氢气.
解答 解:A.Al2H6与水反应生成氢氧化铝和氢气,该反应中H元素化合价由-1价、+1价变为0价,所以属于氧化还原反应,其中一种产物是氢氧化铝,生成的氢气既是氧化产物还是还原产物,故A正确;
B.Al2H6在空气中燃烧生成Al的氧化物和H的氧化物,所以产物是氧化铝和水,故B正确;
C.根据图知,该分子结构对称,正负电荷重心重合,为非极性分子,故C错误;
D.氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高,能和水反应生成氢氧化铝和氢气,所以氢铝化合物可能成为未来的储氢材料和火箭燃料,故D正确;
故选C.
点评 本题考查铝的化合物性质,侧重考查学生获取信息利用信息解答问题能力,熟练掌握元素化合物知识即可解答,注意该化合物是分子晶体而不是离子晶体,为易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
3.下列说法正确的是( )
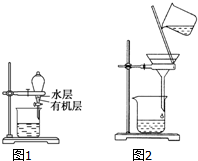

| A. | 分离乙醇和乙酸乙酯的混合物,所用玻璃仪器为分液漏斗、烧杯 | |
| B. | 用如图1所示装置分离CCl4萃取碘水后已分层的有机层和水层 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | 用如图2所示装置除去乙醇中的苯酚 |
10.某有机物A可用于合成药物达菲,其结构简式如图,下列关于A的说法不正确的是( )


| A. | 分子式为C7H6O5 | |
| B. | 和溴水既可以发生取代反应,又可以发生加成反应 | |
| C. | 1 mol该化合物最多可以与含4 mol NaOH的溶液反应 | |
| D. | 既可以和FeCl3溶液发生显色反应,又可以和NaHCO3溶液反应放出CO2气体 |
20.食品香精菠萝酯的生产路线(反应条件略去)如图所示.下列叙述错误的是( )


| A. | 步骤①产物中残留的苯酚可用FeCl3溶液检验 | |
| B. | 步骤②产物中残留的CH2=CHCH2OH可用溴水检验 | |
| C. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| D. | 苯氧乙酸和菠萝酯均可与H2在一定条件下发生反应 |
7.下列与有机物结构、性质相关的叙述错误的是( )
| A. | 乙酸分子中含有羧基,可与NaHCO3溶液反应生成 CO2 | |
| B. | 所有的醇在铜做催化剂加热的条件下,都能与O2 发生氧化 | |
| C. | 甲烷和氯气在光照下的反应与苯的硝化反应的反应类型相同 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有碳碳双键 |
4.二次电池又叫可逆电池,下列电池不属于二次电池的是( )
| A. | 酸性锌锰干电池和碱性锌锰干电池 | B. | 铅蓄电池 | ||
| C. | 氢气燃料电池和甲烷燃料电池 | D. | 镍镉电池和锂电池 |
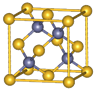 Ⅰ.铬位于第四周期ⅥB族,主要化合价+2,+3,+6,单质硬度大,耐腐蚀,是重要的合金材料.
Ⅰ.铬位于第四周期ⅥB族,主要化合价+2,+3,+6,单质硬度大,耐腐蚀,是重要的合金材料.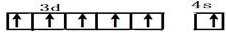 ,CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是非极性(填“极性”或“非极性”)分子.
,CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是非极性(填“极性”或“非极性”)分子.
 .
. 与O2反应制得,写出该反应的化学方程式
与O2反应制得,写出该反应的化学方程式 .
.