题目内容
实验室制氯气时,多余氯气用氢氧化钠溶液吸收,关于该反应的下列说法正确的是( )
| A、Cl2仅作氧化剂 |
| B、NaClO是还原产物 |
| C、每生成1mol NaCl,有1mol Cl2被氧化 |
| D、每转移1mol电子,有0.5mol Cl2被还原 |
考点:氯气的化学性质
专题:卤族元素
分析:氯气与氢氧化钠反应的化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,反应中部分氯元素化合价升高转化为次氯酸钠,部分氯元素化合价降低,转化为钠,消耗1mol氯气,转移电子数为1mol,据此解答.
解答:
解:A.氯气在应中部分氯元素化合价升高,做还原剂,部分部分氯元素化合价降低,做氧化剂,故A错误;
B.氯气在应中部分氯元素化合价升高转化为NaClO,所以次氯酸钠为氧化产物,故B错误;
C.每生成1mol NaCl,转移1mol电子,有0.5mol氯气被氧化,故C错误;
D.反应中每转移1mol电子,有0.5mol Cl2被还原,故D正确;
故选:D.
B.氯气在应中部分氯元素化合价升高转化为NaClO,所以次氯酸钠为氧化产物,故B错误;
C.每生成1mol NaCl,转移1mol电子,有0.5mol氯气被氧化,故C错误;
D.反应中每转移1mol电子,有0.5mol Cl2被还原,故D正确;
故选:D.
点评:本题考查了氯气的性质,题目难度不大,准确分析元素化合价的变化,依据氧化还原反应的规律即可解答.

练习册系列答案
相关题目
除去甲烷气体中含有的少量乙烯,最好选用下列试剂中的( )
| A、蒸馏水 |
| B、溴的四氯化碳溶液 |
| C、浓硫酸 |
| D、酸性KMnO4溶液 |
下列原子或原子团中,不属于官能团的是( )
| A、氯原子 | B、羟基 | C、硝基 | D、苯环 |
下列叙述的乙炔的结构和性质中,既不同于乙烯,也不同于乙烷的是( )
| A、存在不饱和键 |
| B、不易发生取代反应,易发生加成反应 |
| C、分子中的所有原子都处在同一条直线上 |
| D、能使酸性KMnO4溶液褪色 |
某电化学装置如图,下列说法正确的是( )
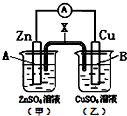

| A、若X是盐桥,则电子由B电极经外电路流向A电极 |
| B、若X是铜条,则A电极的电极反应式是:Zn2++2e-═Zn |
| C、若X是石墨条,则乙池溶液的pH会减小 |
| D、若X是锌条,则A电极的质量会减小 |
已知25℃时有关弱酸的电离平衡常数:
则下列说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、等物质的量浓度的各溶液 pH 关系为:pH( NaCN)>pH(Na2CO3)>pH( CH3COONa) |
| B、浓度均为0.2mol/L NaHCO3和 Na2CO3溶液中,存在的粒子种类不相同 |
| C、0.4mol?L-1 HCN 溶液与 0.2mol?L-1 NaOH 溶液等体积混合后,所得溶液中:c(Na+)>c(OH-)>c(H+) |
| D、25℃时,pH=4且浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液中:c(Na+)+c(H+)>c(CH3COO-)+c(CH3COOH) |
下列化学方程式,能用于工业上冶炼金属镁的是( )
A、2Na+MgCl2
| ||||
B、MgCl2 (熔化)
| ||||
C、2MgO
| ||||
D、MgO+C
|
对于0.1mol?L-1 NH4Cl溶液,下列说法正确的是( )
| A、溶液中c(Cl-)=c(NH4+)+c(NH3?H2O) |
| B、c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| C、c(NH4+)+c(OH-)=c(Cl-)+c(H+) |
| D、通入少量HCl,c(NH4+)和c(Cl-)均增大 |
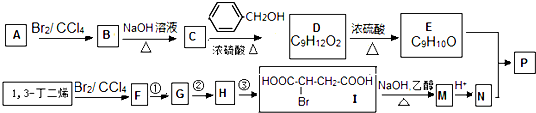
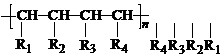 nCH=CH+nCH=CH
nCH=CH+nCH=CH