题目内容
将NO2装入带活塞的密闭容器中,当反应2NO2(g) N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是()
N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是()
 N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是()
N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是()| A.升高温度,气体颜色加深,则此反应为吸热反应 |
| B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅 |
| C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍 |
| D.恒温恒容时,充入少量惰性气体,压强增大,平衡向右移动,混合气体的颜色变浅 |
C
试题分析:A.升高温度,气体颜色加深,说明升高温度化学平衡向逆反应方向移动。根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,逆反应方向是吸热反应,所以则此反应的正反应为放热反应。错误。B.慢慢压缩气体体积,使体系的压强增大,各物质的浓度增大。由于该反应的正反应是气体体积减小的反应,所以增大压强化学平衡向右移动,但平衡移动的四很微弱的,只能减弱这种改变,总的来说各物质的浓度与原来比大。所以混合气体颜色变深。错误。C.慢慢压缩气体体积,若体积减小一半,压强增大,如果平衡不移动,压强为原来的二倍,现在体系的压强小于原来的两倍。说明增大压强,平衡向正反应方向发生了移动。正确。D.恒温恒容时,充入少量惰性气体,压强增大,但由于反应混合物中各物质的浓度没有发生变化,所以平衡不移动,混合气体的颜色不变。错误。

练习册系列答案
相关题目

 和Cr
和Cr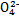 ),其流程为:Cr
),其流程为:Cr Cr2
Cr2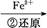 Cr3+
Cr3+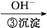 Cr(OH)3↓
Cr(OH)3↓ Cr2
Cr2 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq) Cr2
Cr2 4X(g)+nY(g)。反应完全后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值是
4X(g)+nY(g)。反应完全后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值是 SO3(g)+NO(g) ΔH<0
SO3(g)+NO(g) ΔH<0 XC(g) + 2D(g)。当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则下列叙述不正确的是
XC(g) + 2D(g)。当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则下列叙述不正确的是  3C(g)的下列叙述中,能说明反应已达到平衡的是
3C(g)的下列叙述中,能说明反应已达到平衡的是 MgO(s)+CO2(g)+SO2(g) ΔH>0
MgO(s)+CO2(g)+SO2(g) ΔH>0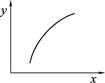
 2HI (g)达到平衡的标志是
2HI (g)达到平衡的标志是