题目内容
【题目】下列说法不正确的是( )
A.乙烯分子中的 σ键和π键比例为 5:1
B.某元素气态基态原子的逐级电离能(kJmol﹣1)分别为 738、1451、7733、10540、13630、17995、21703, 当它与氯气反应时可能生成的阳离子是 X2+
C.Na、P、Cl 的电负性依次增大
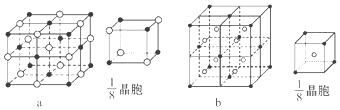
D.向配合物[TiCl(H2O)5]Cl2H2O 溶液中加入足量的 AgNO3 溶液,所有 Cl-均被完全沉淀
【答案】D
【解析】
A. 共价单键是σ键,共价双键中含有1个π键1个σ键,共价三键中含有2个π键1个σ键,乙烯的结构式为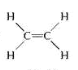 ,含有5个σ键,1个π键,σ键和π键比例为 5:1,A正确;
,含有5个σ键,1个π键,σ键和π键比例为 5:1,A正确;
B. 该元素第三电离能剧增,最外层应有2个电子,表现+2价,当它与氯气反应时最可能生成的阳离子是X2+,B正确;
C.Na、P、Cl 为同周期元素,同周期元素,从左到右电负性依次增大,所以Na、P、Cl电负性依次增大,C正确;
D. 向配合物 [TiCl(H2O)5]Cl2H2O 溶液中加入足量的 AgNO3 溶液,外界Cl-被完全沉淀,D错误;
故答案为:D。

【题目】现使用酸碱中和滴定法测定市售白醋的浓度
Ⅰ.实验步骤
(1)配制待测白醋溶液,用________(填仪器名称)量取1.00mL食用白醋,在______(填仪器名称)中用水稀释后转移到100mL________(填仪器名称)中定容,摇匀即得待测白醋溶液
(2)量取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴酚酞作指示剂
(3)读取盛装0.1000mol·L-1NaOH溶液的碱式滴定管的初始读数
(4)滴定,判断滴定终点的现象是__________达到滴定终点,停止滴定,并记录NaOH溶液的最终读数,重复滴定3次。
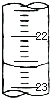
(5)如图是某次滴定时的滴定管中的液面,其读数为______ mL.
Ⅱ.实验记录
实验数据(mL)/滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(6)甲同学在处理数据时计算得:c(市售白醋)=______mol·L-1
(7)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果_____(填“偏小”“偏大”或“无影响”):观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的白醋浓度的测定值______(填“偏小”“偏大”或“无影响”)。