��Ŀ����
����Ŀ���������������������������Ҫԭ��֮һ���������������ж��ַ�����
(1)Ŀǰ��Ӧ����㷺���������������ѳ�������NH3����ԭ������ѧ��Ӧ�ɱ�ʾΪ��
2NH3(g)+NO(g)+NO2(g)== 2N2(g)+3H2O(g) ��H��0
�ٸ÷�Ӧ�У���Ӧ��������_____(�>������<����=��)��������������
�ڵ��÷�Ӧ��2mol N2(g)����ʱ��ת�Ƶ��ӵ����ʵ���Ϊ__mol��
�۸÷�Ӧ�У���ԭ��Ϊ______(�ѧʽ�������������뻹ԭ�����������Ϊ______________��
(2)Ҳ�������ü������ԭ���������֪��
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H=-574kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ��H=-867kJ/mol
��CH4(g)��NO(g)��ԭΪN2(g)���Ȼ�ѧ����ʽ��_________________��
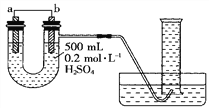
(3)��������ClO2���������������Ⱦ����Ӧ��������(���ַ�Ӧ�����������ȥ)��![]()
��ӦI�IJ����л�������ǿ�����ɣ�������һ��ǿ��Ϊ���ᣬ��������NO3���ʵ�����ȣ�����ѧ��Ӧ����ʽΪ______����Ӧ��������22.4L N2(��״��)��������ClO2______g��
(4)����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ���
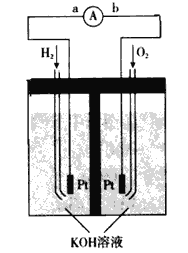
������ȼ�ϵ�ص�����ת����Ҫ��ʽ��________������ʱ��������Ϊ________����a��b�ͼ�ͷ��ʾ����
�ڸ����ĵ缫��ӦʽΪ__________________��
�۵缫����Ʋ��۵�ԭ��Ϊ____________________��
���𰸡� �� 6 NH3 1 :1 CH4��g��+4NO��g��=2N2��g��+CO2��g��+2H2O��g����H=��1160kJ��mol��1 2NO + ClO2 + H2O = NO2 + HNO3 + HCl 135 ��ѧ�������� b��a H2��2e��+2OH��=2H2O ����缫��λ�������H2��O2�ķ�����������Ӧ����
�����������������������Ҫ���鷴Ӧ�ȵļ��㼰ԭ��ط�Ӧԭ����
(1) ���÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ��������>��������������
�����÷�Ӧ��2mol N2(g)����ʱ��N2��3e-��ת�Ƶ��ӵ����ʵ���Ϊ6mol��
���÷�Ӧ�У���ԭ��ΪNH3�����������뻹ԭ�����������Ϊ1:1��
(2)����֪�������Ȼ�ѧ����ʽ������עΪ�٢ڣ�2��-�ٵ�CH4(g)��NO(g)��ԭΪN2(g)���Ȼ�ѧ����ʽ��CH4��g��+4NO��g��=2N2��g��+CO2��g��+2H2O��g����H=��1160kJ��mol��1 ��
(3)���������غ㶨�ɿ����ж���һ��ǿ����HCl����ѧ��Ӧ����ʽΪ2NO + ClO2 + H2O = NO2 + HNO3 + HCl����Ӧ��������22.4L��1mol N2(��״��)��2ClO2��2NO2��N2��������ClO22mol��135 g��
(4) ������ȼ�ϵ�ص�����ת����Ҫ��ʽ�ǻ�ѧ�������ܣ�O2���ڵĵ缫������������ʱ��������Ϊb��a ��
��H 2���ڵĵ缫�Ǹ����������ĵ缫��ӦʽΪH2��2e��+2OH��=2H2O��
���缫����Ʋ��۵�ԭ��Ϊ����缫��λ�������H2��O2�ķ�����������Ӧ������

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�