��Ŀ����
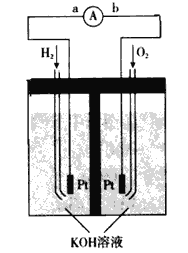
����Ŀ��I��������ͼװ�����ⶨijԭ��ع���ʱ��ij��ʱ����ͨ�����ߵĵ��ӵ����ʵ�������Ͳ�Ĺ��Ϊ1000 mL����ѡ��ĵ缫�����д�ͭƬ�ʹ�пƬ����ش��������⣺
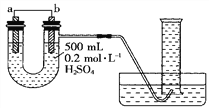
��1��b�缫����Ϊ__________����缫��ӦʽΪ_________________________��
��2������Ͳ���ռ���672 mL(��״����)����ʱ��ͨ�����ߵĵ��ӵ����ʵ���Ϊ__________����ʱa�缫��������__________g��
II��ijͬѧ����ϡ������п��ȡ������ʵ���У����ּ�����������ͭ��Һ�ɼӿ��������������ʡ���ش��������⣺
��1������ʵ���з�����Ӧ�����ӷ���ʽ�У�_____________________________________________��
��2������ͭ��Һ���Լӿ������������ʵ�ԭ����_________________________________________��
��3��Ҫ�ӿ�����ʵ����������������ʣ����ɲ�ȡ�Ĵ�ʩ��_____________________�������֣���
���𰸡� ��ͭƬ 2H����2e��===H2�� 0.06 mol 1.95 Zn + 2H+ ==Zn2+ + H2����Zn + Cu2+ == Zn2+ + Cu CuSO4��Zn��Ӧ������Cu��Zn�Լ�������Һ�γ�Cu/Znԭ��أ��ӿ����������������� ���߷�Ӧ�¶ȡ��ʵ����������Ũ�ȡ�����п���ıȱ������
��������I�������⣬���װ��ͼ������Ͳ�ռ�������Ȼ��ͨ���������������������¼ʱ�䣬���ij��ʱ��������������ʵ������������ij��ʱ����ͨ�����ߵĵ��ӵ����ʵ�����
��1��������������b�˲�����������������b�缫����Ϊ��ͭƬ���缫��ӦʽΪ2H����2e��=H2����
��2��672 mL(��״����)���������ʵ���Ϊ��0.672L��22.4L/mol=0.03mol������ת�Ƶ���Ϊ0.06mol������Zn + 2H+ =Zn2+ + H2���ɵã�a�缫��Zn������0.03mol����0.03mol��65g/mol=1.95g��
II����1����ΪCu2+�������Ա�H+��ǿ�����Լ�����������ͭ��Һ��Zn�������ͭ��Ӧ��Ȼ�������ᷴӦ����Ӧ���йط���ʽΪ��Zn + Cu2+ =Zn2+ + Cu��Zn + 2H+ =Zn2+ + H2����
��2��Zn������ͭ��Ӧ�û���ͭ����п�γ�ԭ��أ���ѧ��Ӧ���ʼӿ졣
��3������Һ�н��еĻ�ѧ��Ӧ��Ӱ���䷴Ӧ���ʵ����ػ��д������¶ȡ�Ũ�ȼ�����������С�ȣ�����Ҫ�ӿ�����ʵ����������������ʣ����ɲ�ȡ�Ĵ�ʩ�У����߷�Ӧ�¶ȡ��ʵ����������Ũ�ȡ�����п���ı�����ȡ�

 ��У����ϵ�д�
��У����ϵ�д�