题目内容
等体积、pH相同的氨水与NaOH溶液,下列说法正确的是
| A.分别加水稀释相同的倍数,稀释后两溶液pH仍相同 |
| B.NaOH溶液中水电离产生的c(OH-)较小 |
| C.用等浓度的盐酸完全中和,消耗盐酸体积相等 |
| D.加入少量NH4Cl(s),pH均减小 |
D
试题分析:A、因为加水稀释能促进弱碱的电离平衡向右移动,所以分别加水稀释相同的倍数,稀释后两溶液pH:氨水 > NaOH,错误;B、因为氨水和NaOH溶液的pH相同,即碱电离出的OH?浓度相同,所以对水的电离平衡的抑制作用也相同,水电离产生的OH?离子浓度相同,错误;C、氨水的电离程度小,则氨水的浓度远远大于NaOH浓度,所以用等浓度的盐酸完全中和,氨水消耗盐酸体积多,错误;D、加入少量NH4Cl(s),抑制氨水的电离平衡,NH4Cl能与NaOH反应生成弱碱,所以pH均减小,正确。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目



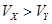
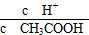 C.c(H+)·c(OH-) D.
C.c(H+)·c(OH-) D.