题目内容
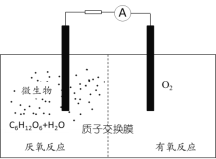
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
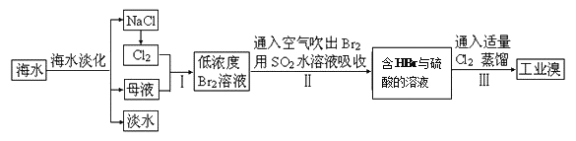
(1)除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序正确的是__________。
A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
(2)制备钠单质的方法之一是将熔融NaCl进行电解,写出电解化学方程式:
______________________________________________________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是____________。写出步骤Ⅱ中发生反应的化学方程式:_______________________________________________。
(4)某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59 ℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下实验装置:
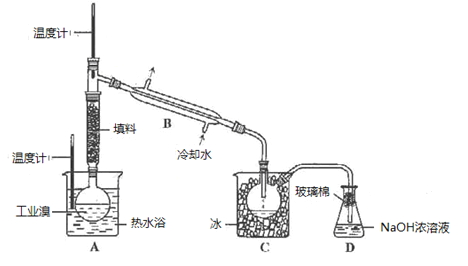
①图中仪器B的名称是________,冷却水的出口为____(填“甲”或“乙”)。
②C中液体的颜色为__________________。
③D装置的作用是__________________。
(5)已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中的Cl-、Br-、I-的物质的量之比变成4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的________。(填选项)
A.![]() B. C.
B. C.![]() D.
D.![]()
【答案】 BC 2NaCl(熔融) ![]() 2Na+Cl2↑ 提高溴的富集程度 Br2+SO2+2H2O===2HBr+H2SO4 直形冷凝管 甲 深棕红色或红棕色 吸收尾气 C
2Na+Cl2↑ 提高溴的富集程度 Br2+SO2+2H2O===2HBr+H2SO4 直形冷凝管 甲 深棕红色或红棕色 吸收尾气 C
【解析】(1)要先除SO42-离子,然后再除Ca2+离子,碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,至于加NaOH除去Mg2+离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,只要将三种离子除完了,然后过滤即可,最后加盐酸除去过量的氢氧根离子碳酸根离子,所以正确的操作顺序为:A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸,最后加入的氯化钡溶液中钡离子不能除去,故A错误;B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,故B正确;C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸,故C正确;D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸,顺序中加入的氯化钡溶液中钡离子无法除去,故D错误;故答案为:BC;
(2)制备钠单质的方法之一是将熔融NaCl进行电解,写出的电解化学方程式为:2NaCl(熔融)![]() 2Na+Cl2↑,故答案为:2NaCl(熔融)
2Na+Cl2↑,故答案为:2NaCl(熔融)![]() 2Na+Cl2↑;
2Na+Cl2↑;
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,目的是低浓度的Br2溶液在提取时消耗过多的原料和能源,转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素,步骤Ⅱ中发生反应是二氧化硫吸收溴单质发生反应:Br2+SO2+2H2O═H2SO4+2HBr,故答案为:富集溴元素;Br2+SO2+2H2O═H2SO4+2HBr;
(4)①由装置图可知,提纯溴利用的原理是蒸馏,仪器B为冷凝管,冷凝水应从下端进,即从乙进,冷却水的出口为甲,故答案为:冷凝管;甲;
②控制温度59℃,使溴单质挥发,通过冷凝得到呈深红棕色或红棕色的液态溴单质,故答案为:深棕红色或红棕色;
③进入D装置的物质为溴蒸汽,溴蒸汽有毒,避免污染环境,最后进行尾气吸收,故答案为:吸收尾气;
(5)已知还原性I->Br->Cl-,反应后I-有剩余,说明Br-浓度没有变化,通入的Cl2只与I-发生反应,设原溶液中含有2molCl-,3molBr-,4molI-,通入Cl2后,它们的物质的量之比变为4:3:2,则各离子物质的量分别为:4molCl-,3molBr-,2molI-,Cl-增加了2mol,则需1molCl2,则通入的Cl2物质的量是原溶液中I-物质的量的![]() ,故选C。
,故选C。

 阅读快车系列答案
阅读快车系列答案