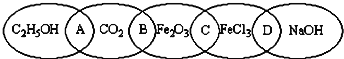��Ŀ����
����Ŀ����1����(N2H4)���ӿ���ΪNH3�����е�һ����ԭ�ӱ���NH2(����)ȡ���γɵ���һ�ֵ����⻯�NH3���ӵ����幹����________��N2H4�����е�ԭ�ӹ�����ӻ�������________��
��2����OH����Ϊ�ȵ������һ�ַ���Ϊ________________(�ѧʽ)��N��O��F�ĵ�һ�������ɴ�С��˳��Ϊ________________��
��3���� H2O�����У�H��O��H�ļ�����________��H������H2O�γ�H3O����H3O����H��O��H���DZ�H2O��H��O��H���Ǵ�ԭ��Ϊ_________________________________________��
���𰸡� ������ sp3 HF F��N��O 105o H2O����ԭ����2�Թµ��Ӷԣ�H3O������ԭ��ֻ��1�Թµ��Ӷԣ��ų�����С
��������(1)����NH3�����У���3��N-H������һ�Թµ��Ӷԣ����ݼ۲���ӶԻ���ģ���жϷ��ӿռ乹��Ϊ�����ͣ���N2H4�У���ԭ�Ӽ۲���Ӷ���Ϊ![]() =4�����Ե�ԭ�ӵ��ӻ���ʽΪsp3�ӻ����ʴ�Ϊ�������ͣ�sp3��
=4�����Ե�ԭ�ӵ��ӻ���ʽΪsp3�ӻ����ʴ�Ϊ�������ͣ�sp3��
(2)��OH����Ϊ�ȵ������һ�ַ���ΪHF��ͬһ����Ԫ�صĵ�һ����������ԭ�����������������������ƣ�����IIA��͵�VA��Ԫ�صĵ�һ�����ܴ�������Ԫ�أ�����N��O��F����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ��F��N��O���ʴ�Ϊ��HF��F��N��O��
(3)ˮ����ΪV�Σ��� H2O�����У�H��O��H�ļ�����105�����µ��Ӷ�֮����ų������ڹµ��ӶԺ��õ��Ӷ�֮����ų�����ˮ����������ֻ��һ�Թµ��Ӷԡ�ˮ�����к������Թµ��Ӷԣ�ˮ�����������µ��Ӷ��ų�������ˮ���������йµ��Ӷ��빲�ۼ�֮����ų���������H3O+��H-O-H���DZ�H2O��H-O-H���Ǵʴ�Ϊ��105����H2O����ԭ����2�Թµ��Ӷԣ�H3O������ԭ��ֻ��1�Թµ��Ӷԣ��ų�����С��

����Ŀ����Դ�������������������ᷢչ������ء�
��1��һ���¶��£��������ݻ���Ϊ2L���ܱ������У��ֱ�����Ӧ��CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)��H=-49.0kJ��mol-1������������£�
CH3OH(g)��H2O(g)��H=-49.0kJ��mol-1������������£�
���� | �� | �� |
��Ӧ��Ͷ���� | 1molCO2(g)��3molH2(g) | 1molCH3OH(g����1molH2O(g) |
ƽ��ʱc(CH3OH) | c1 | c2 |
ƽ��ʱ�����仯 | �ų�29.4kJ | ����akJ |
�����������˵���÷�Ӧһ���ﵽƽ��״̬����_________������ĸ����
a��v(CO2)����=v(CH3OH)���� b��������ܶȲ�����ʱ��ı�
c��CO2��CH3OH��Ũ��֮�Ȳ�����ʱ��ı� d�������ƽ����Է�������������ʱ��ı�
�������������䣬�ﵽƽ������в������H2ת���ʵIJ�����_________������ĸ����
a�������¶� b����������H2 c���Ƴ��״� d�������������
��cl_________c2(����>������<������=��)��a=_________��
�ܸ��¶��·�Ӧ��ƽ�ⳣ��K=_________�������з�Ӧ10sʱ�ﵽƽ�⣬��0��10s�ڼ��е�ƽ����Ӧ����v(H2)=_________��
��2����֪��Ӧ��2NO2(����ɫ)![]() N2O4(��ɫ)��H��0����һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ����__________������ĸ����
N2O4(��ɫ)��H��0����һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ����__________������ĸ����
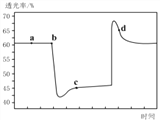
A��b��IJ�����ѹ��ע����
B��d�㣺v����v��
C��c����a����ȣ�c(NO2)����c(N2O4)��С
D������������ϵ�¶ȱ仯����û��������ʧ����Tb��Tc