题目内容
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
(1)Ⅰ.将钠、镁、铝各1 mol分别投入到足量同浓度的盐酸中,试预测实验结果:与盐酸反应最剧烈;与盐酸反应产生的气体最多(填名称).
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为:
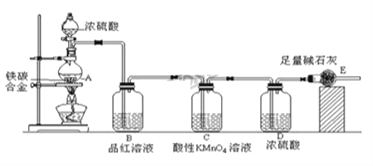
(3)Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律 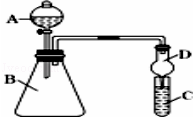
仪器A的名称为 , 干燥管D的作用为 .
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉﹣碘化钾混合溶液,观察到C中溶液的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用溶液吸收尾气,此吸收反应的离子方程式;
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入C 中干扰试验,应在两装置间添加装有溶液的洗气瓶除去.
【答案】
(1)钠;铝
(2)S2﹣+Cl2═S↓+2Cl﹣
(3)分液漏斗;防倒吸
(4)变蓝;NaOH;Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
(5)有白色沉淀生成;饱和NaHCO3
【解析】解:Ⅰ.(1)同周期从左向右,随着原子序数的递增,元素的金属性逐渐减弱,钠、镁、铝属于同一周期,且原子序数逐渐增大,或根据金属活动性顺序表金属活泼性顺序可知:金属活泼性:钠>镁>铝,所以相同条件下与盐酸反应最激烈的是钠,反应速率最慢的是铝;生成1mol氢气需要得到2mol电子,1mol钠都失去1mol电子,1mol镁失去2mol电子,而1mol铝失去3mol电子,所以生成氢气最多的是金属铝,所以答案是:钠;铝; (2)氯气氧化性强于硫单质,所以氯气能够与硫离子反应生成硫,反应的离子方程式为:S2﹣+Cl2═S↓+2Cl﹣ , 所以答案是:S2﹣+Cl2═S↓+2Cl﹣;Ⅱ.(3)A的名称是分液漏斗,球形干燥管D球形部分具有较大空间,能起缓冲作用,能够防止倒吸,可以避免C中液体进入锥形瓶中,所以答案是:分液漏斗;防倒吸;(4)KMnO4与浓盐酸反应生成氯气,2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,氯气与淀粉碘化钾混合溶液反应生成碘单质,反应离子方程式为:2I﹣+Cl2═I2+2Cl﹣ , 碘遇淀粉试液变蓝色,故C中溶液变为蓝色;过量的氯气会逸散到空气中,污染环境,可用NaOH溶液吸收,反应离子方程式为:2OH﹣+Cl2═Cl﹣+ClO﹣+H2O,所以答案是:变蓝;NaOH;Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;(5)因碳酸比硅酸强,二氧化碳可与硅酸钠反应生成硅酸沉淀,溶液变浑浊,氯化氢具有挥发性,所以生成的二氧化碳中含有HCl,HCl能和硅酸钠反应而使溶液变浑浊,所以干扰实验结果,需要将二氧化碳中的氯化氢除掉,根据氯化氢与碳酸氢钠反应,而二氧化碳不反应,可以在B和C之间增加装有饱和NaHCO3溶液的洗气瓶, 所以答案是:有白色沉淀生成;饱和NaHCO3 .
【考点精析】掌握非金属在元素周期表中的位置及其性质递变的规律是解答本题的根本,需要知道在目前已知的112种元素中,非金属元素有22种,除H外非金属元素都位于周期表的右上方(H在左上方).F是非金属性最强的元素.