题目内容
19.下列各组内的离子,在溶液中不能大量共存的是( )| A. | H+、SO42、Ba2+、NO3- | B. | Ca2+、H+、NO3、Cl | ||
| C. | Mg2+、K+、NO3-、Cl- | D. | K+、Na+、Mg2+、SO42- |
分析 根据离子之比不能结合生成水、气体、沉淀等,离子之间不能发生氧化还原反应,则能大量共存,以此来解答.
解答 解:A中SO42、Ba2+反应生成沉淀而不能大量共存,而B、C、D中离子之间不发生任何反应,可大量共存,故选A.
点评 本题考查离子的共存,为高考常见题型,侧重学生思维严密性的考查,熟悉复分解反应及氧化还原反应即可解答,选项A为解答的难点,题目难度不大.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
9.已知钡的活性处于钾和钠之间,下列反应可以实现的是( )
| A. | 钡可以从氯化钾溶液中置换出钾 | |
| B. | 钡与冷水剧烈反应置换出氢气 | |
| C. | 钡可以从氯化钠溶液中置换出钠 | |
| D. | 在溶液中钡离子可以氧化金属锌,使之成为锌离子 |
4.某研究性学习小组设想将少量Cl2通入Fe2+和I-的混合溶液中,探究Fe2+和I-的还原性强弱.
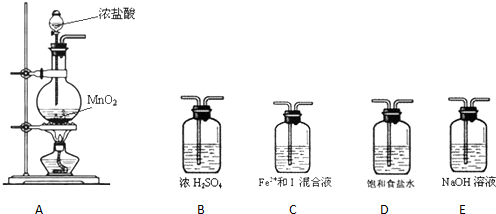
【提出假设】假设1:Fe2+还原性比I-强.假设2:I-还原 性比Fe2+强.假设3:一样强
【验证假设】(1)设计如下几种装置进行实验:
实验 必须的装置是A→C→E(按Cl2气流方向的顺序填写)
(2)实验开始后,控制通入 少量氯气,通过观察混合溶液颜色的变化不能(填“能”或“不能”)判断反应的先后顺序.
(3)请在下表中写出实验步骤及预期现象和结论.
(4)为了实验成功,必须控制各物质的量.该小组称取3.04gFeSO4,同时称取3.32gKI固体,溶于水中.为了验证上述假设,通入的Cl2体积 最多不能超过0.224L(标准状况).
【思考与交流】
(5)有同学质疑,上述实验只能验证Cl2分别与Fe2+和I-反应的速率大小,并不能证明Fe2+和I-还原性的强弱.于是提出另一方案:往KI溶液中滴入某溶液,如果能发生反应,即可证明I-的还原性强于Fe2+,该反应的离子方程式是2I-+2Fe3+=I2+2Fe2+.

【提出假设】假设1:Fe2+还原性比I-强.假设2:I-还原 性比Fe2+强.假设3:一样强
【验证假设】(1)设计如下几种装置进行实验:
实验 必须的装置是A→C→E(按Cl2气流方向的顺序填写)
(2)实验开始后,控制通入 少量氯气,通过观察混合溶液颜色的变化不能(填“能”或“不能”)判断反应的先后顺序.
(3)请在下表中写出实验步骤及预期现象和结论.
| 实验步骤 | 预期现象和结论 | |
| 取少量反应后的混合溶液分置于A、B两试管中; 往A中滴加KSCN溶液; 往B中滴加淀粉溶液. |
|
【思考与交流】
(5)有同学质疑,上述实验只能验证Cl2分别与Fe2+和I-反应的速率大小,并不能证明Fe2+和I-还原性的强弱.于是提出另一方案:往KI溶液中滴入某溶液,如果能发生反应,即可证明I-的还原性强于Fe2+,该反应的离子方程式是2I-+2Fe3+=I2+2Fe2+.
5.下列各装置图对应的叙述正确的是( )
| A. | 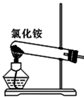 实验室用装置制取氨气 | |
| B. |  装置X若为CCl4,可用于吸收氨气并防止倒吸 | |
| C. |  装置可用于制备氢氧化亚铁并观察其颜色 | |
| D. |  装置是原电池,铁电极为负极,发生氧化反应 |
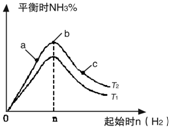 某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)反应的影响,实验结果可表示成如图所示的规律(图中T表示温度,n表示物质的量):
某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)反应的影响,实验结果可表示成如图所示的规律(图中T表示温度,n表示物质的量):