题目内容
【题目】下列操作达不到预期目的是( )
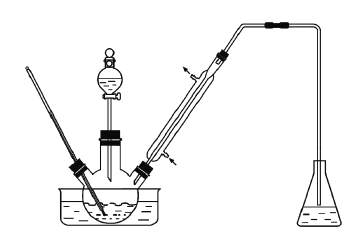
![]() 用乙醇与3mol/L的H2SO4混合共热制乙烯;
用乙醇与3mol/L的H2SO4混合共热制乙烯;
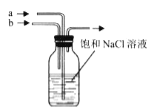
![]() 将饱和食盐水滴入盛有电石的烧瓶中制乙炔;
将饱和食盐水滴入盛有电石的烧瓶中制乙炔;
![]() 将苯和溴水混合后加入Fe粉制溴苯;
将苯和溴水混合后加入Fe粉制溴苯;
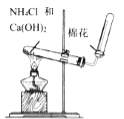
![]() 分馏石油时将温度计的水银球位于蒸馏烧瓶的支管口处,实验室制乙烯则是伸入到混合液中;
分馏石油时将温度计的水银球位于蒸馏烧瓶的支管口处,实验室制乙烯则是伸入到混合液中;
![]() 制硝基苯时,应先加浓硝酸,再加浓硫酸,待液体冷却后再加苯;
制硝基苯时,应先加浓硝酸,再加浓硫酸,待液体冷却后再加苯;
![]() 将
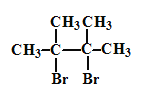
将![]() 与NaOH的醇溶液共热制备CH3-CH=CH2
与NaOH的醇溶液共热制备CH3-CH=CH2
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】A
【解析】
①3mol/L的H2SO4不是浓硫酸,不能与乙醇反应生成乙烯,不能达到预期,符合题意,①正确;
②饱和食盐水滴入盛有电石的烧瓶中,反应平稳,可制备乙炔,与题意不符,②错误;
③苯和溴水不反应,则将苯和液溴混合后加入Fe粉制溴苯,不能达到预期,符合题意,③正确;
④分馏时测定馏分的温度,而制备乙烯测定反应液的温度,则分馏石油时将温度计的水银球位于蒸馏烧瓶的支管口处,实验室制乙烯则是伸入到混合液中,与题意不符,④错误;
⑤制硝基苯时,先加密度小的酸,再加密度大的酸,最后加苯,苯易挥发,则制硝基苯时,应先加浓硝酸,再加浓硫酸,待液体冷却后再加苯,与题意不符,⑤错误;
⑥醇与浓硫酸加热发生消去反应,则将![]() 与浓硫酸共热制备CH3-CH=CH2,符合题意,⑥正确;
与浓硫酸共热制备CH3-CH=CH2,符合题意,⑥正确;
综上所述,答案为A。

【题目】已知:CH3CH2CH2CH2OH→CH3CH2CH2CHO
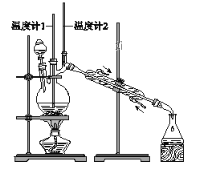
利用下图装置用正丁醇合成正丁醛。相关数据如下:
物质 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是( )
A. 为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B. 向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
C. 反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D. 当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物