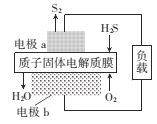
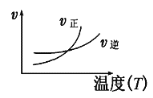
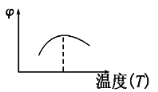
题目内容
【题目】将1 mol I2(g)和2 mol H2置于某2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) ![]() 2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。
2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。
(1)达到平衡时,I2(g)的物质的量浓度为______________mol·L-1。
(2)若改变反应条件,在甲条件下w(HI)的变化如图曲线(Ⅱ)所示,在乙条件下w(HI)的变化如图曲线(Ⅲ)所示。则甲条件可能是______________,乙条件可能是______________。(填入下列条件的序号)
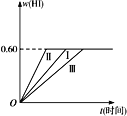
①恒容条件下,升高温度 ②恒容条件下,降低温度 ③恒温条件下,缩小反应容器体积 ④恒温条件下,扩大反应容器体积 ⑤恒温恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g),b mol H2(g)和c molHI(g)(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是_____________________________。
【答案】0.05③⑤④ 4a+c=2b
【解析】
(1)达到平衡时,HI的体积分数w(HI)=0.6,利用“三段式”计算I2(g)的物质的量浓度;(2)恒容条件下,改变温度,平衡移动,HI的体积分数改变;减压反应速率减慢、加压反应速率加快,反应前后气体系数和不变,改变压强平衡不移动,HI的体积分数不变;适当催化剂能加快反应速率,但不能使平衡移动,HI的体积分数不变;(3)根据等效平衡原理分析。
(1)达到平衡时,HI的体积分数w(HI)=0.6,
I2(g)+H2(g) ![]() 2HI(g)
2HI(g)
始 0.5 1 0
转 x x 2x
平 0.5-x 1-x 2x
![]()
X=0.45
所以达到平衡时,I2(g)的物质的量浓度为0.5-0.45=0.05mol·L-1;(2)恒容条件下,改变温度,平衡移动,HI的体积分数改变;减压反应速率减慢、加压反应速率加快,反应前后气体系数和不变,改变压强平衡不移动,HI的体积分数不变;适当催化剂能加快反应速率,但不能使平衡移动,HI的体积分数不变;根据图像可知由曲线(Ⅰ)变为曲线(Ⅱ),反应速率加快,但平衡没移动,所以甲条件可能是加压或加入适当催化剂,故选③⑤;由曲线(Ⅰ)变为曲线(Ⅲ),反应速率减慢,但平衡没移动,所以乙条件可能是减压,故选④;(3)若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g),b mol H2(g)和c molHI(g)(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,即为等效平衡;加入a mol I2(g),b mol H2(g)和c molHI(g),相当于加入(a+![]() ) mol I2(g)、(b+
) mol I2(g)、(b+![]() ) mol H2(g);I2(g)+H2(g)
) mol H2(g);I2(g)+H2(g) ![]() 2HI(g)反应前后气体系数和不变,投料比等于原平衡的投料比即为等效平衡,则(a+
2HI(g)反应前后气体系数和不变,投料比等于原平衡的投料比即为等效平衡,则(a+![]() ):(b+
):(b+![]() ) =1:2,4a+c=2b。
) =1:2,4a+c=2b。

 快捷英语周周练系列答案
快捷英语周周练系列答案【题目】下列设计的实验方案能达到相应实验目的的是
选项 | 实验目的 | 实验方案 |
A | 探究化学反应的限度 | 取5mL0.1mol/LKI溶液,滴加0.1molLFeCl3溶液5~6滴,充分反应,可根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应 |
B | 探究浓度对化学反应速率的影响 | 用两支试管各取5ml.0.1mo/L的KMnO4溶液,分别加入2mL0.1mol/L和10.2mol/L的H2C2O4(草酸)溶液,记录溶液褪色所需的时间 |
C | 证明海带中含有碘元素 | 将海带剪碎、加蒸馏水浸泡,取滤液加几滴稀硫酸和1mLH2O2,再加入几滴淀粉溶液,溶液变蓝 |
D | 验证CH3COONa 溶液中存在水解平衡 | 取CH3COONa溶液于试管中并加入几滴酚酞试剂,再加入醋酸铵固体(其水溶液呈中性),观察溶液颜色变化 |
A. A B. B C. C D. D
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得:
2CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O +CO2↑。
I.制备碳酸亚铁:装置如图所示。
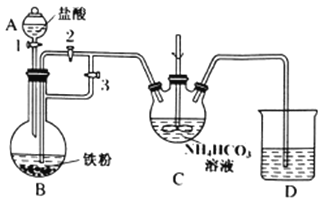
(1)C的名称是___________。
(2)清洗仪器,检查装置气密性,A中加入盐酸,B中加入铁粉,C中加入NH4HCO3溶液。为顺利达成实验目的,上述装置中活塞的打开和关闭顺序为:关闭活塞______,打开活塞______;加入足量盐酸后,关闭活塞1,反应一段时间后,关闭活塞____,打开活塞_____。C中发生的反应的离子方程式为_______________。
Ⅱ.制备乳酸亚铁晶体:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸。
(3)加入少量铁粉的作用是______________。从所得溶液中获得乳酸亚铁晶体所需的实验操作是隔绝空气低温蒸发,________、干燥。
Ⅲ.乳酸亚铁晶体纯度的测量:
(4)若用KMnO4滴定法测定样品中Fe2+的量进而计算纯度时,发现结果总是大于100%,其原因可能是_____________________。
(5)经查阅文献后,改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取5.760g样品,溶解后进行必要处理,用容量瓶配制成250mL溶液,每次取25.00mL,用0.1000mol/LCe(SO4)2标准溶液滴定至终点,记录数据如下表。
滴定次数 | 0.1000mol/LCe(SO4)2标准溶液体积/mL | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 19.85 |
2 | 0.12 | 21.32 |
3 | 1.05 | 20.70 |
则产品中乳酸亚铁晶体的纯度为_________(以质量分数表示)。