题目内容
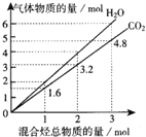
【题目】两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法正确的是( )
A. 该混合气体一定含有乙烯
B. 该混合气体一定含甲烷和乙炔
C. 在常温下,该混合气体与足量氧气混合,完全燃烧后恢复至常温燃烧前后总体积不变
D. 若混合气体由CH4和C2H4组成,则其体积比为2:3
【答案】D
【解析】由图可知两种气态烃的平均组成为C1.6H4,根据碳原子平均数可知,混合气体一定含有CH4,由氢原子平均数可知,另一气态烃中氢原子数目为4,碳原子数目大于1.6,不超过4。A、混合气体一定含有CH4,由氢原子平均数可知,另一气态烃中氢原子数目为4,可能含有C2H4,或含有C3H4等,A错误;B、C2H2中氢原子数目为2,氢原子数目小于4,不可能含有C2H2,B错误;C、如果生成的水为气体,两种气态烃的平均组成为C1.6H4,H原子数目为4,燃烧前后总体积不变,但在常温下水是液体,C错误;D、若混合气体由CH4和C2H4组成,令甲烷物质的量为xmol、乙烯为ymol,两种气态烃的平均组成为C1.6H4,根据平均C原子数目可知,(x+2y)/(x+y)=1.6,整理得x:y=2:3,D正确;答案选D。

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
【题目】下列实验操作中,可达到对应实验目的的是( )
实验操作 | 实验目的 | |
A | 苯和溴水混合后加入铁粉 | 制溴苯 |
B | 某有机物与溴的四氯化碳溶液混合 | 确认该有机物含碳碳双键 |
C | 将 | 检验该有机物中的溴原子 |
D | 乙醇与酸性高锰酸钾溶液混合 | 检验乙醇具有还原性 |
A. A B. B C. C D. D