题目内容
已知反应3H2+N2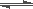 2NH3为放热反应,由此推断出 ( )
2NH3为放热反应,由此推断出 ( )
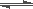 2NH3为放热反应,由此推断出 ( )
2NH3为放热反应,由此推断出 ( )| A.氢气和氮气在常温常压下,不需要任何能量就可以迅速发生反应 |
| B.3mol氢气和1mol氮气所具有的总能量低于2mol氨气所具有的总能量 |
| C.断裂1molN≡N键和3molH—H键吸收的能量小于形成6molN—H键所放出的能量 |
| D.氢气和氮气是高能极不稳定的物质,氨气是低能且非常稳定的物质 |
C
试题分析:A.任何反应的发生都有个反应物中化学键断裂和生成物中的化学键形成的过程,因此该反应发生时要吸收热量。错误。B.由于该反应是放热反应,所以3mol氢气和1mol氮气所具有的总能量搞于2mol氨气所具有的总能量。错误。C.断裂1molN≡N键和3molH—H键吸收的能量小于形成6molN—H键所放出的能量,所以多余的能量就释放出来,因此该反应是放热反应。正确。D.氢气和氮气中的化学键键能较高,是较稳定的物质。由于氮气与氢气合成氨气的反应是放热反应,所以产生的氨分子也是比较稳定的物质。错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 CO2(g) ΔH=-437.3 kJ?mol-1
CO2(g) ΔH=-437.3 kJ?mol-1 CO(g) + H2(g) ΔH= kJ?mol-1。如果该反应ΔS=+133.7 J·K-1·mol-1 该反应在常温(25 ℃)下能否自发进行?(△G=△H-T△S) (填“能”或“不能”,并写出判断依据).
CO(g) + H2(g) ΔH= kJ?mol-1。如果该反应ΔS=+133.7 J·K-1·mol-1 该反应在常温(25 ℃)下能否自发进行?(△G=△H-T△S) (填“能”或“不能”,并写出判断依据).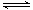 2NH3 △H="a" kJ·mol-1。试根据表中所列键能数据估算a的数值为 。
2NH3 △H="a" kJ·mol-1。试根据表中所列键能数据估算a的数值为 。 HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
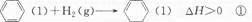
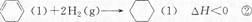
 2SO3(g)
2SO3(g) 2SO3(g) △H= 。
2SO3(g) △H= 。