题目内容
【题目】已知A、B、C是中学化学中最常见的三种有机物,D是高分子化合物,常用来制造食品和药品包装袋,已知这四种物质之间存在如图所示关系:
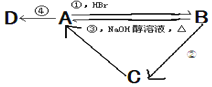
(1)写出反应类型:①___,③____,④____。
(2)反应②的条件是____。
(3)写出化学方程式:B→C:___,A→D:___。
【答案】加成反应 消去反应 加聚反应 NaOH水溶液、加热 CH3CH2Br+NaOH![]() CH3CH2OH+NaBr nCH2=CH2
CH3CH2OH+NaBr nCH2=CH2![]()
【解析】
D是高分子化合物,常用来制造食品和药品包装袋,可知D为![]() ,结合图中转化可知,A为CH2=CH2,A与HBr发生加成反应生成CH3CH2Br,B发生消去生成A,则B发生水解反应生成C为CH3CH2OH,C发生消去反应生成A,据此分析解答。
,结合图中转化可知,A为CH2=CH2,A与HBr发生加成反应生成CH3CH2Br,B发生消去生成A,则B发生水解反应生成C为CH3CH2OH,C发生消去反应生成A,据此分析解答。
(1)①为乙烯的加成反应,③为卤代烃的消去反应,④为乙烯的加聚反应,故答案为:加成反应;消去反应;加聚反应;
(2)反应②为卤代烃的水解反应,反应条件是NaOH水溶液、加热,故答案为:NaOH水溶液、加热;
(3)![]() 的化学反应为CH3CH2Br+NaOH
的化学反应为CH3CH2Br+NaOH![]() CH3CH2OH+NaBr,
CH3CH2OH+NaBr,![]() 的化学反应为
的化学反应为![]() ,故答案为:CH3CH2Br+NaOH
,故答案为:CH3CH2Br+NaOH![]() CH3CH2OH+NaBr;
CH3CH2OH+NaBr;![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
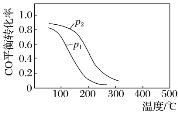
小学生10分钟应用题系列答案【题目】(1).用合成气生成甲醇的反应:CO(g)+2H2(g) ![]() CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①ΔH________(填“>”“<”或“= ”)0。
②写出一条可同时提高反应速率和CO转化率的措施:________________________。
③下列说法正确的是________(填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=__________________。
⑤ 200 ℃时,该反应的平衡常数K=________。向上述200 ℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡________(填“正向”“逆向”或“不”)移动。